Đề thi giữa HK2 môn Hóa học 12 năm 2021-2022
Trường THPT Ngô Gia Tự
-
Câu 1:
Phương pháp nhiệt nhôm dùng để điều chế kim loại:
A. Dùng điều chế các kim loại đứng sau H.
B. Dùng điều chế các kim loại đứng sau Al.
C. Dùng điều chế các kim loại dễ nóng chảy.
D. Dùng điều chế các kim loại khó nóng chảy.
-
Câu 2:
Để làm sạch lớp cặn trong các dụng cụ đun và chứa nước nóng, người ta thường dùng:
A. nước vôi trong
B. giấm ăn
C. ancol etylic
D. dung dịch muối ăn
-
Câu 3:
Có thể dùng dung dịch nào sau đây để phản ứng hoàn toàn một mẫu gang ?
A. Dung dịch HCl
B. Dung dịch H2SO4 loãng
C. Dung dịch NaOH
D. Dung dịch HNO3 đặc, nóng
-
Câu 4:
Cho Br2 vào dung dịch CrCl3 trong môi trường NaOH thì sản phẩm thu được có chứa:
A. CrBr3.
B. Na[Cr(OH)4].
C. Na2CrO4.
D. Na2Cr2O7.
-
Câu 5:
Cho các tác hại sau:
1, Gây ngộ độc nước uống.
2, Có tính tẩy màu, ăn mòn da tay
3, Làm mất tính tẩy rửa của xà phòng, làm hư hại quần áo.
4, Làm hỏng các dung dịch pha chế. Làm thực phẩm lâu chín và giảm mùi vị thực phẩm.
5, Gây hao tốn nhiên liệu và không an toàn cho các nồi hơi, làm tắc các đường ống dẫn nước.
6, Sử dụng nước cứng để ăn uống dễ dẫn đến các bệnh lí như sỏi thận, sỏi mật.
Số tác hại mà nước cứng gây ra là
A. 3
B. 4
C. 5
D. 6
-
Câu 6:
Phương pháp thường được áp dụng để chống ăn mòn kim loại là
A. Phương pháp bảo vệ bề mặt, phương pháp điện hóa.
B. Phương pháp nhiệt luyện, thủy luyện.
C. Phương pháp điện phân nóng chảy, điện phân dung dịch.
D. Tất cả các phương pháp trên.
-
Câu 7:
Cho từ từ đến dư kim loại Na vào dung dịch có chứa muối FeCl3. Sau phản ứng thu được kết tủa Y và dung dịch X chứa
A. FeCl3, NaOH
B. NaCl, NaOH
C. NaOH
D. Fe(OH)3, NaCl
-
Câu 8:
Nhận xét nào sau đây là không đúng ?
A. Các kim loại kiềm thổ có tính khử mạnh
B. Tính khử của các kim loại kiềm thổ tăng dần từ Be đến Ba
C. Tính khử của các kim loại kiềm thổ yếu hơn kim loại kiềm trong cùng chu kì
D. Be, Mg, Ca, Sr, Ba đều phản ứng với nước ở nhiệt độ thường nên gọi là kim loại kiềm thổ
-
Câu 9:
Trong không khí ẩm, kim loại đồng bị bao phủ bởi lớp màng
A. CuO (màu đen).
B. CuS (màu đen).
C. CuCl2 (màu xanh).
D. CuCO3.Cu(OH)2 (màu xanh).
-
Câu 10:
Tính chất vật lí nào sau đây của sắt khác với các đơn chất kim loại khác ?
A. Tính dẻo, dễ rèn.
B. Dẫn điện và dẫn nhiệt.
C. Là kim loại nặng.
D. Có tính nhiễm từ.
-
Câu 11:
Vì sao những vật bằng nhôm hàng ngày tiếp xúc với nước dù ở nhiệt độ nào cũng không xảy ra phản ứng ?
A. Nhôm là kim loại không tác dụng với nước
B. Trên bề mặt vật được phủ một lớp nhôm oxit mỏng, bền, ngăn cách vật với nước
C. Do nhôm tác dụng với nước tạo lớp nhôm hiđroxit không tan bảo vệ cho nhôm
D. Nhôm là kim loại hoạt động không mạnh
-
Câu 12:
Cho hỗn hợp gồm Fe và Mg vào dung dịch AgNO3, khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm hai muối) và chất rắn Y (gồm một kim loại). Hai muối trong X là
A. Mg(NO3)2 và Fe(NO3)2.
B. AgNO3 và Mg(NO3)2.
C. Fe(NO3)3 và Mg(NO3)2.
D. Cả A và C đều đúng
-
Câu 13:
Khi điện phân dung dịch CuCl2, ở catot xảy ra
A. sự khử ion Cu2+
B. sự oxi hóa ion Cu2+
C. sự oxi hóa ion Cl-
D. sự khử ion Cl-
-
Câu 14:
Kim loại nào sau đây không phải kim loại kiềm
A. Ca
B. K
C. Cs
D. Li
-
Câu 15:
Trong các oxit sau : CuO; Al2O3; SO2. Hãy cho biết chất nào chỉ phản ứng được với bazơ và chất nào phản ứng được cả với axit và bazơ ?
A. SO2; CuO
B. CuO; Al2O3
C. SO2; Al2O3
D. CuO; SO2
-
Câu 16:
Trong quá trình hoạt động của pin điện hoá Fe-Cu nồng độ của các ion trong dung dịch biến đổi như thế nào ?
A. Nồng độ ion Cu2+ tăng dần và nồng độ Fe2+ tăng dần
B. Nồng độ ion Fe2+ giảm dần và nồng độ Cu2+ giảm dần
C. Nồng độ ion Fe2+ tăng dần và nồng độ Cu2+ giảm dần
D. Nồng độ ion Fe2+giảm dần và nồng độ Cu2+ tăng dần
-
Câu 17:
Cho dãy: R → RCl2 → R(OH)2 → R(OH)3 → Na[R(OH)4].
R có thể là kim loại nào sau đây?
A. Al
B. Cr
C. Fe
D. Al, Cr
-
Câu 18:
Trong ăn mòn điện hóa, cực âm xảy ra
A. sự oxi hóa, kim loại ở điện cực tan ra.
B. sự oxi hóa và có kim loại bám vào điện cực.
C. sự khử và có kim loại bám vào điện cực.
D. sự oxi hóa
-
Câu 19:
X là kim loại thuộc nhóm IIA. Cho 1,7 gam hỗn hợp gồm kim loại X và Zn tác dụng với lượng dư dung dịch HCl, sinh ra 0,672 lít khí H2 (ở đktc). Mặt khác, khi cho 1,9 gam X tác dụng với lượng dư dung dịch H2SO4 loãng, thì thể tích khí hiđro sinh ra chưa đến 1,12 lít (ở đktc). Kim loại X là
A. Ba.
B. Ca.
C. Sr.
D. Mg.
-
Câu 20:
Hoà tan a gam Cu và Fe (Fe chiếm 40% về khối lượng) bằng 30 ml dung dịch HNO3 60% (D = 1,4 g/ml). Sau khi phản ứng xảy ra hoàn toàn thu được chất rắn X cân nặng 0,65a gam, dung dịch Y và 3,36 lít hỗn hợp khí NO và NO2 (đktc). Cô cạn Y thì số gam muối thu được là
A. 36 gam.
B. 22,5 gam.
C. 45 gam.
D. 49,5 gam.
-
Câu 21:
Cho 4 kim loại Al, Fe, Mg, Cu và 4 dung dịch ZnSO4, AgNO3, CuCl2, Al2(SO4)3. Kim loại khử được cả 4 dung dịch muối đã cho là
A. Fe.
B. Mg.
C. Al.
D. Cu.
-
Câu 22:
Điện phân dung dịch CuSO4 nồng độ 0,5M với điện cực trơ trong thì thu được 1 gam Cu. Nếu dùng dòng điện một chiều có cường độ 1A, thì thời gian điện phân tối thiểu có giá trị gần nhất là
A. 50 phút 15 giây.
B. 40 phút 15 giây.
C. 40 phút 45 giây.
D. 50 phút 45 giây.
-
Câu 23:
Điện phân với các điện cực trơ dung dịch hồn hợp gồm 0,2 mol CuSO4 và 0,12 mol HCl trong thời gian 2000 giây với dòng điện có cường độ là 9,65A (hiệu suất của quá trình điện phân là 100%). Khối lượng Cu thoát ra ở catot và thể tích khí (đktc) thoát ra ở anot là
A. 3,2 gam và 0,448 lít.
B. 8,0 gam và 0,672 lít.
C. 6,4 gam và 1,792 lít.
D. 6,4 gam và 1,120 lít.
-
Câu 24:
Điện phân dung dịch gồm a mol CuSO4 và 2a mol NaCl sau khi ở catot bắt đầu thoát khí thì dừng lại. Chất tan trong dung dịch thu được sau điện phân là
A. CuSO4;Na2SO4.
B. CuSO4; NaCl.
C. Na2SO4.
D. H2SO4; Na2SO4.
-
Câu 25:
Cho luồng khí CO (dư) đi qua 9,1 gam hỗn hợp gồm CuO và Al2O3 nung nóng đến khi phản ứng hoàn toàn, thu được 8,3 gam chất rắn. Khối lượng CuO có trong hỗn hợp ban đầu là
A. 0,8 gam.
B. 8,3 gam.
C. 2,0 gam.
D. 4,0 gam.
-
Câu 26:
Cho 1,82 g một kim loại kiềm tác dụng hết với 48,44 gam nước, sau phản ứng thu được 2,912 lít khí H2 (đktc) và dung dịch X. Kim loại kiềm và nồng độ phần trăm dung dịch X là
A. Li; 44%.
B. Na; 31,65 %.
C. Li; 12,48 %.
D. Na; 44%.
-
Câu 27:
Hòa tan 5,9 gam hỗn hợp X gồm K và Ca vào nước dư, sau phản ứng thu được 2,24 lít khí H2. Khối lượng Ca có trong hỗn hợp X là
A. 3,9 gam.
B. 2 gam.
C. 4,8 gam.
D. 4 gam.
-
Câu 28:
Sục khí CO2 từ từ cho đến dư vào 200 ml dung dịch hỗn hợp NaOH 2M và Ca(OH)2 1M thu được dung dịch A. Cô cạn dung dịch A rồi nhiệt phân đến khối lượng không đổi thu được m gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 41,2.
B. 32,4.
C. 20.
D. 44,8.
-
Câu 29:
Thổi từ từ khí CO2 đến dư vào dung dịch chứa 0,12 mol Ca(OH)2 . Sự phụ thuộc của số mol kết tủa thu được vào số mol CO2 phản ứng được biểu điễn theo đồ thị sau:
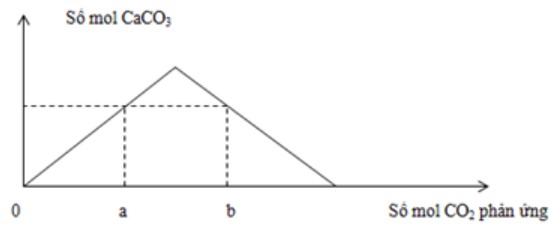
Mối quan hệ của a và b là:
A. b = 0,24 - a
B. b = 0,24 + a
C. b = 0,12 + a
D. b = 2a
-
Câu 30:
Cho 0,85 lít dung dịch NaOH 1M vào dung dịch chứa 0,1 mol Al2(SO4)3 và 0,1 mol H2SO4 đến khi phản ứng hoàn toàn, thu được m gam kết tủa. Giá trị của m là:
A. 11,7.
B. 3,9.
C. 7,8.
D. 15,6.
-
Câu 31:
Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch Al2(SO4)3 hiện tượng quan sát được là
A. xuất hiện kết tủa trắng rồi tan hết và tạo thành dung dịch trong suốt.
B. xuất hiện kết tủa trắng và không tan.
C. xuất hiện kết tủa trắng và có khí bay ra.
D. xuất hiện kết tủa trắng sau đó tan một phần.
-
Câu 32:
Nung hỗn hợp A gồm 22,8 gam Cr2O3 và m gam Al. Sau khi phản ứng hoàn toàn thu được 33,6 gam hỗn hợp rắn X. Cho toàn bộ X phản ứng với axit HCl dư thoát ra V lít H2 (đktc). Giá trị của V là:
A. 10,08.
B. 7,84.
C. 4,48.
D. 13,44.
-
Câu 33:
Nhận biết lọ đựng Fe và Fe2O3 bằng phương pháp hóa học trong 3 lọ hóa chất đựng hỗn hợp các chất rắn sau Fe và FeO; Fe và Fe2O3; FeO và Fe2O3 chỉ cần dùng loại thuốc thử nào dưới đây
A. dd HCl
B. dd H2SO4 loãng
C. dd HNO3 đặc nguội
D. Tất cả các phương án đều đúng
-
Câu 34:
Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X có tỉ khối so với khí hiđro bằng 18,8. Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là
A. 9,40 gam.
B. 11,28 gam.
C. 8,60 gam.
D. 47,00 gam.
-
Câu 35:
Thổi khí NH3 dư đi qua 10 gam CrO3 đun nóng đến phản ứng hoàn toàn thu được chất rắn màu xanh lục có khối lượng là
A. 0,52 gam.
B. 0,68 gam.
C. 7,60 gam.
D. 1,52 gam.
-
Câu 36:
Hỗn hợp X gồm Na, Ba và Al2O3 (trong đó oxi chiếm 24,78% khối lượng). Hòa tan hết 29,05 gam X trong nước dư, thu được dung dịch Y và 4,48 lít H2 (đktc). Cho từ từ dung dịch Z chứa hỗn hợp HCl 0,8M và H2SO4 0,1M vào X đến khi thu được lượng kết tủa lớn nhất, lọc kết tủa và nung đến khối lượng không đổi, thu được m gam chất rắn. Giá trị gần nhất của m là
A. 26,3
B. 25,2.
C. 24,6.
D. 25,8.
-
Câu 37:
Hòa tan hoàn toàn a gam hỗn hợp gồm x mol AgNO3 và y mol Cu(NO3)2 vào nước, thu được dung dịch X. Cho một lượng Cu dư vào X thu được dd Y có chứa b gam muối. Cho một lượng Fe dư vào Y, thu được dung dịch Z có chứa c gam muối. Biết các phản ứng xảy ra hoàn toàn 2b = a + c. Tỉ lệ x : y là:
A. 8 : 1.
B. 9 : 1.
C. 1 : 8.
D. 1 : 9.
-
Câu 38:
Hòa tan hết m gam hỗn hợp gồm Na, Na2O, Ba, BaO vào nước, thu được 0,06 mol khí H2 và dung dịch X. Hấp thụ hết 0,128 mol khí CO2 vào dung dịch X, thu được dung dịch Y (chỉ chứa các muối) và kết tủa Z. Chia dung dịch Y làm 2 phần bằng nhau:
+ Cho từ từ phần 1 vào 200 ml dung dịch HCl 0,24M thấy thoát ra 0,03 mol khí CO2.
+ Nếu cho từ từ 200 ml dung dịch HCl 0,24M vào phần 2 thấy thoát ra 0,024 mol khí CO2. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 8,368.
B. 12,272.
C. 10,352.
D. 11,312.
-
Câu 39:
Điện phân dung dịch AgNO3 với điện cực trơ, sau một thời gian thu được dung dịch X chứa 2 chất tan có cùng nồng độ (mol/lít), và thấy khối lượng dung dịch giảm đi 11,6 gam so với ban đầu. Cho tiếp 3,36 gam bột Fe vào dung dịch X, thu được dung dịch Y và chất rắn Z và khí NO ( sản phẩm khử duy nhất của N5+). Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối trong dung dịch Y là:
A. 14,8.
B. 14,21.
C. 10,24.
D. 13,64.
-
Câu 40:
Hòa tan hoàn toàn 3,92 gam bột Fe vào 44,1 gam dung dịch HNO3 50% thu được dung dịch X(không có ion NH4+, bỏ qua sự hòa tan của các khí trong nước và sự bay hơi của nước). Cho X phản ứng với 200ml dung dịch chứa đồng thời KOH 0,5M và NaOH 1M. Sau khi các phản ứng xảy ra hoàn toàn, lọc bỏ kết tủa thu được dung dịch Y. Cô cạn Y thu được chất rắn Z. Nung Z đến khối lượng không đổi, thu được 20,56 gam hỗn hợp chất rắn khan. Nồng độ phần trăm của Fe(NO3)2 trong dung dịch X là
A. 37,18%.
B. 37,52%.
C. 38,71%.
D. 35,27%.











