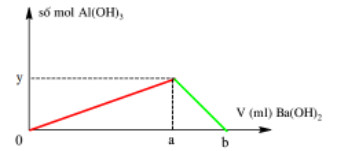
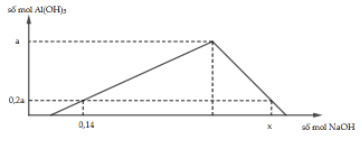
Cho a mol Al vào hỗn hợp chứa b mol HCl thu được dung dịch Y chứa 2 chất tan có cùng nồng độ mol. Thêm từ từ dung dịch NaOH vào dung dịch Y ta có đồ thị sau:
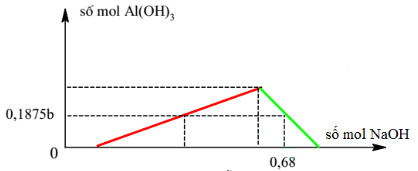
Cho a mol Al phản ứng với dung dịch hỗn hợp chứa 0,15b mol FeCl3 và 0,2b mol CuCl2. Sau khi phản ứng kết thúc thu được x gam chất rắn. Giá trị của x là:
Suy nghĩ và trả lời câu hỏi trước khi xem đáp án
Lời giải:
Báo saiDung dịch Y chứa nAlCl3 = nHCl dư = a mol
Bảo toàn nguyên tố Cl ta có: nCl- = 3a + a = 4a = b mol (1)
Khi nNaOH = 0,68 mol: kết tủa bị hòa tan một phần:
Do đó: nOH- = nH+ + 4.nAl3+ - nAl(OH)3 ⟹ 0,68 = a + 4a - 0,1875b (2)
Giải hệ (1) và (2) ta có: a = 0,16 và b = 0,64
Vậy nFeCl3 = 0,15b = 0,096 mol; nCuCl2 = 0,2b = 0,128 mol
Sau phản ứng dung dịch thu được chứa Cl- 0,544 mol; Al3+ 0,16 mol;
Bảo toàn điện tích ta suy ra nFe2+ = 0,032 mol
Vậy chất rắn gồm Fe (0,096 - 0,032 = 0,064 mol) và Cu: 0,128 mol
→ mchất rắn = 0,128.64 + 0,064.56 =11,776 gam.