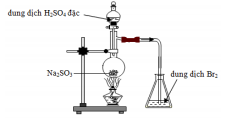
Đốt cháy hoàn toàn 12,8g lưu huỳnh thu được khí A. Lượng khí A được hấp thu hết bởi 88,8 gam dung dịch Ca(OH)2 25%. Tìm C% của các chất trong dung dịch thu được sau phản ứng.
Chính xác
Xem lời giải
Suy nghĩ và trả lời câu hỏi trước khi xem đáp án
ADSENSE
Lời giải:
Báo sainS = 12,8 : 32 = 0,4 mol
mCa(OH)2 = 22,2 gam
nCa(OH)2 = 22,3 : 74 = 0,3 mol
S + O2 → SO2 (mol)
0,4 → 0,4
mCa(OH)2 = (88,8.25) : 100 = 22,2 gam
1 < T = nSO2/nCa(OH)2 < 2, phản ứng tạo thành hai muối Đặt số mol của CaSO3 và Ca(HSO3)2 lần lượt là x và y
Ta có
x + y = 0,3 và x + 2y = 0,4 ⇒ x = 0,2 và y = 0,1
mCaSO3 = 0, 2.120 = 24(g)
mdd sau= 0,4.64 + 88,8 – 24 = 90,4(g)
C% = 22,35%
ADMICRO
YOMEDIA
ZUNIA9