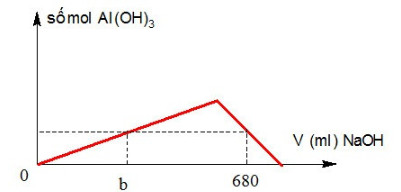
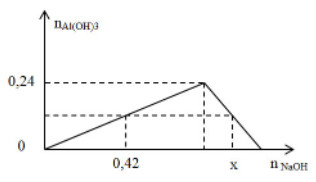
Khi nhỏ NaOH vào dung dịch hỗn hợp gồm AlCl3 và FeCl3, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
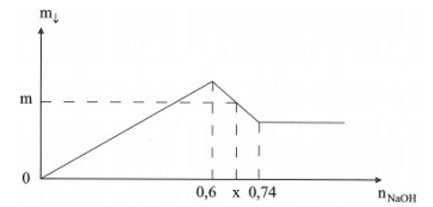
Khi x = 0,66 mol thì giá trị của m (gam) là?
Suy nghĩ và trả lời câu hỏi trước khi xem đáp án
Lời giải:
Báo saiĐặt nAlCl3 = a mol và nFeCl3 = b mol
→ Số mol cực đại của Al(OH)3 là a mol; số mol cực đại của Fe(OH)3 là b mol
Khi Al(OH)3 và Fe(OH)3 đạt cực đại thì: nOH- = 3a + 3b = 0,6 mol
Khi nNaOH = 0,74 mol thì số mol kết tủa không đổi → Tại đó Al(OH)3 tan hết tạo NaAlO2
Suy ra nNaOH = 4a + 3b = 0,74 mol
Giải hệ trên ta được a = 0,14 mol và b = 0,06 mol
Khi nNaOH = x mol thì Fe(OH)3 đạt cực đại và Al(OH)3 bắt đầu tan ra
→ nNaOH = 3.nFe(OH)3 + 4.nAl3+ - nAl(OH)3
Với x = 0,66 mol suy ra 0,66 = 3.b + 4.a - nAl(OH)3 → nAl(OH)3 = 0,08 mol
Vậy khối lượng kết tủa là m = mFe(OH)3+ mAl(OH)3 = 0,06.107 + 0,08.78 =12,66 gam.