Trắc nghiệm Tính chất vật lý của Lưu huỳnh dioxit- lưu huỳnh Trioxit Hóa Học Lớp 10
-
Câu 1:
Kết luận nào sau đây không phù hợp với công thức cấu tạo của SO2?
-
Câu 2:
Cho các phản ứng hóa học sau: \(\left( a \right){\rm{ }}S{\rm{ }} + {\rm{ }}{O_2}\;\mathop \to \limits^{{t^o}} \;\;S{O_2};(b)S{\rm{ }} + {\rm{ 3}}{F_2}\;\mathop \to \limits^{{t^o}} \;\;S{F_6};(c)S + Hg\;\mathop \to \limits^{{t^o}} SHg;\) (d) S + 6HNO3 đặc \(\mathop \to \limits^{{t^o}} \;\;\) H2SO4 + 6NO2 + 2H2O. Số phản ứng trong đó S thể hiện tính khử là
-
Câu 3:
Những hóa chất để nhận biết Na2S, K2CO3, BaCl2, Na2SO3, NaCl lần lượt là gì?
-
Câu 4:
Những chất phản ứng được với H2SO4 đặc nguội là gì?
-
Câu 5:
Tìm X biết ở điều kiện thường X là một chất khí, có khả năng tan tốt trong nước tạo ra dung dịch làm đổi màu quỳ tím thành đỏ. X còn được dùng làm chất tẩy trắng giấy, bột giấy, chống nấm mốc cho lương thực, thực phẩm.
-
Câu 6:
Hãy tìm ra nhận định đúng?
1. SO2 vừa là chất oxi hóa, vừa là chất khử.
2. Phản ứng giữa H2S và SO2 dùng để thu hồi S trong các khí thải.
3. Ozon có tính khử mạnh và khử được Ag ở điều kiện thường.
4. Dẫn khí O3 qua dung dịch KI có hồ tinh bột, dung dịch có màu xanh.
5. NaHSO3 có tên natri hiđrosunfit.
6. FeCO3 tác dụng với H2SO4 loãng và H2SO4 đặc cho cùng 1 loại muối.
-
Câu 7:
Cho 4,8 gam bột lưu huỳnh tác dụng với 6,5 gam bột kẽm. Sau khi phản ứng với %H = 80% được hỗn hợp chất rắn X. Hòa tan X trong HCl dư thu được bao nhiêu lít khí?
-
Câu 8:
Tính V biết 1 lượng Ca(OH)2 vừa đủ tác dụng với V lít khí SO2 (đktc) thu được 6 gam kết tủa. Lọc bỏ kết tủa cho tiếp một lượng dung dịch Ca(OH)2 dư vào phần nước lọc thì thu thêm 3 gam kết tủa nữa.
-
Câu 9:
Tính V biết 0,1 mol mỗi chất Fe, FeS và FeS2 vào H2SO4 đặc nóng thu được V lít khí (đktc) SO2 sản phẩm khử duy nhất.
-
Câu 10:
Cho thí nghiệm
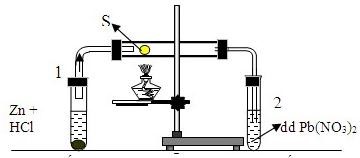
-
Câu 11:
Ý kiến đúng về muối sunfat?
-
Câu 12:
Khí không thể làm khô bằng H2SO4 đặc là gì?
-
Câu 13:
SO2 có thể gây khó thở cho người bị hen suyễn, gây các bệnh về hô hấp và làm cho bệnh tim càng nặng hơn. SO2 phản ứng với những hạt này sẽ tụ tập trong phổi và gắn kết với nhau gây khó thở và dẫn đến nguy cơ tử vong. Có thể kết luận gì về tính chất của SO2?
-
Câu 14:
Tìm X biết khi tan trong nước dung dịch X làm quỳ tím chuyển màu đỏ và có tính tẩy màu?
-
Câu 15:
Dãy gồm chất có tính oxi hóa khi phản ứng với SO2 là dãy nào bên dưới đây?
-
Câu 16:
Khí SO2 (sinh ra từ việc đốt các nhiên liệu hóa thạch, quặng sunfua) là một trong những chất gây ô nhiễm môi trường, do SO2 trong không khí sinh ra nguyên nhân nào sau đây?
-
Câu 17:
Cần dùng bao nhiêu mol KOH tác dụng vừa đủ với 6,72 lít khí SO2 để thu được 39,8 gam hỗn hợp muối.
-
Câu 18:
Hãy tính m muối thu được khi cho 4,48 lít SO2 (đktc) vào 150 ml NaOH 2M?
-
Câu 19:
Tìm thành phần muối thu được khi cho 2,24 lit khí SO2 (đkc) vào 100 ml dung dịch NaOH 1,5M?
-
Câu 20:
Thể tích dung dịch NaOH 2M tối thiểu để hấp thụ hết 5,6 lit khí SO2 (đkc) là
-
Câu 21:
Xác định tỉ khối hơi của Y so với H2 biết đun nóng 4,8 gam Mg với 4,8 gam S trong điều kiện không có không khí, thu được hỗn hợp rắn X. Hòa tan X vào HCl dư, thu được hõn hợp khí Y.
-
Câu 22:
Tính %Fe cho biết đun 20 gam X gồm Fe và S thu được hỗn hợp rắn A. Cho A vào HCl thu được 6,72 lít (đktc) Y?
-
Câu 23:
Cho 4,48 lít SO2 (đktc) vào 150 ml dung dịch NaOH 2M, thu được dung dịch chứa bao nhiêu gam muối.
-
Câu 24:
Tính m biết đốt cháy hoàn toàn m gam FeS2 bằng một lượng O2 vừa đủ, thu được khí X. Hấp thị hết X vào 2 lít dung dịch chứa Ba(OH)2 0,1M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa.
-
Câu 25:
Hạn chế khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch gì?
-
Câu 26:
Tính giá trị a biết hấp thụ 6,72 lít khí SO2 (đktc) vào a mol KOH, thu được 39,8 gam hỗn hợp muối.
-
Câu 27:
Tính m kết tủa thu được khi đốt cháy 4,48 g lưu huỳnh rồi cho sản phẩm cháy vào 200 ml Ba(OH)2 0,5M?
-
Câu 28:
Để diệt chuột trong một nhà kho người ta dùng phương pháp đốt lưu huỳnh, đóng kín cửa nhà kho lại. Chuột hít phải khói sẽ bị sưng yết hầu, co giật, tê liệt cơ quan hô hấp dẫn đến bị ngạt mà chết. Chất nào sau đây là nguyên nhân chính gây ra các hiện tượng trên?
-
Câu 29:
Tính %H biết oxi hoá 89,6 lít SO2 (đktc) ở điều kiện thích hợp thu được 240 gam SO3?
-
Câu 30:
Tính V SO2 cần cho vào 200 ml dung dịch KOH 1M để thu được 12 gam muối KHSO3.
-
Câu 31:
Xác định chất tan thu được khi cho 2,24 lít khí SO2 (đktc) vào 300 ml dung dịch NaOH 1M?
-
Câu 32:
Xác định chất làm mất màu dung dịch brom?
-
Câu 33:
Tính %mSO2 trong X biết X gồm hai khí SO2 và CO2 có tỉ khối đối với H2 là 27?
-
Câu 34:
Hiện tượng khi cho SO2 vào dung dịch KMnO4 là gì?
-
Câu 35:
Điều nào diễn ta đúng tính chất của SO2?
(1) SO2 + 2H2S → 3S + 2H2O
(2) SO2+ Br2 + H2O → 2HBr + H2SO4
-
Câu 36:
Tính V biết dẫn SO2 (đktc) vào lượng dư dung dịch Br2, không thấy khí thoát ra. Thêm tiếp dung dịch BaCl2 dư vào dung dịch sau phản ứng, thu được 23,3 gam kết tủa.
-
Câu 37:
Phát biểu đúng?
(a) Sục khí SO2 vào dung dịch NaOH dư tạo ra muối trung hòa Na2SO3.
(b) SO2 vừa có tính khử, vừa có tính oxi hóa.
(c) Khí SO2 là một trong những nguyên nhân chính gây ra mưa axit.
(d) Khí SO2 có màu vàng lục và rất độc.
-
Câu 38:
Để chứng tỏ SO2 là một oxit axit, người ta cho SO2 phản ứng với chất nào?
-
Câu 39:
Tính V khí SO2 thu đươc khi cho 12,8 gam S phản ứng hoàn toàn với O2 dư?
-
Câu 40:
Hãy xác định tính oxi hóa của S trong SO2?
-
Câu 41:
Khẳng định đúng về tính oxi hóa của H2S?
-
Câu 42:
H2S bị oxi hóa thành S khi nào?
1) Dẫn khí H2S qua dung dịch FeCl3
2) Để dung dịch H2S ngoài trời
3) Đốt khí H2S ở điều kiện thiếu oxi
-
Câu 43:
Tính V biết V lít SO2 (đktc) vào 300 ml Ba(OH)2 1M thu được 21,7g kết tủa.
-
Câu 44:
Ý kiến nào sau đây đúng:
Cho a mol SO2 vào dung dịch chứa 1,5a mol KOH.
-
Câu 45:
Cho 6,72 lít SO2 vào brom rồi cho dung dịch thu được tác dụng với BaCl2 dư, tính m kết tủa thu được sau phản ứng?
-
Câu 46:
Tính V cần KOH 2M để hấp thụ hết 0,3 mol SO2 ?
-
Câu 47:
Cho 2,24 lít khí SO2 (đkc) vào 200 ml KOH 1,5M thì thu được những sản phẩm nào?
-
Câu 48:
Tính V biết dẫn V lít (đktc) khí SO2 vào 200 ml KOH 1M được 12 gam muối KHSO3.
-
Câu 49:
Tính m muối tạo thành khi hấp thụ hoàn toàn 12,8g SO2 vào 250ml dung dịch NaOH 1M.
-
Câu 50:
Cách loại bỏ tạp chất SO2 có trong CO2 là gì?












