Đề thi giữa HK1 môn Hóa học 10 CD năm 2022-2023
Trường THPT Nguyễn Trãi
-
Câu 1:
Trong các hiện tượng sau đây hiện tượng nào là hiện tượng vật lí?
A. Lưu huỳnh (sulfur) cháy trong không khí, tạo ra chất khí mùi hắc.
B. Đốt cháy khí methane, thu được khí carbon dioxide và hơi nước.
C. Hòa tan đường vào nước, thu được dung dịch nước đường.
D. Nung đá vôi, thu được vôi sống và khí carbon dioxide.
-
Câu 2:
Nhận định nào sau đây không đúng?
A. Nguyên tử có kích thước vô cùng nhỏ và trung hòa về điện.
B. Lớp vỏ nguyên tử chứa electron mang điện tích âm.
C. Khối lượng nguyên tử hầu hết tập trung ở hạt nhân.
D. Tất cả các hạt nhân nguyên tử đều chứa proton và neutron.
-
Câu 3:
Nguyên tử alminium (kí hiệu: Al) có số hạt mang điện tích dương là 13, số hạt không mang điện là 14. Số hạt electron trong Al là
A. 27
B. 26
C. 13
D. 14
-
Câu 4:
Hạt nhân của nguyên tử X có điện tích là +30,438.10-19 coulomb. Vậy nguyên tử X là
A. Ar (Z = 18).
B. K (Z = 19).
C. Ca (Z = 20).
D. Cl (Z = 17).
-
Câu 5:
Nguyên tử trung hòa về điện vì
A. có tổng số hạt proton bằng tổng số hạt electron.
B. có tổng số hạt electron bằng tổng số hạt neutron.
C. tổng số hạt neutron bằng tổng số hạt proton.
D. được tạo nên bởi các hạt không mang điện.
-
Câu 6:
Nếu hạt nhân nguyên tử có Z hạt proton thì
A. Số đơn vị điện tích hạt nhân là Z+.
B. Điện tích hạt nhân là Z.
C. Số hạt neutron là Z.
D. Tổng số hạt mang điện trong nguyên tử là 2Z.
-
Câu 7:
Một loại nến được làm bằng paraffin, khi đốt nến, xảy ra các quá trình sau:
(1) Paraffin nóng chảy;
(2) Paraffin lỏng chuyển thành hơi;
(3) Hơi paraffin cháy biến đổi thành khí CO2 và hơi nước.
Quá trình nào có sự biến đổi hoá học?
A. (1).
B. (2).
C. (3).
D. (1), (2), (3).
-
Câu 8:
Các hạt cấu tạo nên hạt nhân của hầu hết các nguyên tử là
A. electron và proton.
B. proton và neutron.
C. neutron và electron.
D. electron, proton và neutron.
-
Câu 9:
Trong nguyên tử, loại hạt có khối lượng và mang điện tích âm là
A. hạt nhân.
B. hạt proton.
C. hạt neutron.
D. hạt electron.
-
Câu 10:
Phát biểu nào sau đây không đúng?
A. Điện tích của proton và electron có cùng độ lớn nhưng ngược dấu.
B. Có những nguyên tử không có neutron.
C. Có những nguyên tử không có proton.
D. Khối lượng của proton và neutron xấp xỉ bằng nhau và lớn hơn nhiều khối lượng của electron.
-
Câu 11:
Thành phần nào bị lệch hướng trong trường điện?
A. Neutron.
B. Electron.
C. Nguyên tử hydrogen.
D. Nguyên tử oxygen.
-
Câu 12:
Nguyên tử X có 26 proton trong hạt nhân. Cho các phát biểu sau về X
(1) X có 26 neutron trong hạt nhân.
(2) X có 26 electron ở vỏ nguyên tử.
(3) X có điện tích hạt nhân là + 26.
(4) Khối lượng nguyên tử X là 26 amu.
Trong các phát biểu trên, số phát biểu đúng là
A. 1
B. 2
C. 3
D. 4
-
Câu 13:
Số hiệu nguyên tử cho biết
A. số proton trong hạt nhân nguyên tử.
B. điện tích hạt nhân nguyên tử.
C. số electron trong nguyên tử.
D. cả A, B, C đều đúng.
-
Câu 14:
Một nguyên tử X gồm 16 proton, 16 electron và 16 neutron. Nguyên tử X có kí hiệu là
A. \({}_{{\rm{16}}}^{{\rm{48}}}{\rm{S}}\)
B. \({}_{{\rm{32}}}^{{\rm{16}}}{\rm{Ge}}\)
C. \({}_{{\rm{16}}}^{32}{\rm{S}}\)
D. \({}_{32}^{16}{\rm{S}}\)
-
Câu 15:
Số hạt mang điện trong nguyên tử \({}_{\rm{3}}^{\rm{7}}{\rm{Li}}\) là
A. 3
B. 7
C. 6
D. 4
-
Câu 16:
Đồng vị của cùng một nguyên tố hóa học là những nguyên tử có
A. cùng số proton nhưng khác nhau về số neutron.
B. cùng số neutron nhưng khác nhau về số proton.
C. cùng tổng số proton và neutron nhưng khác nhau về số electron.
D. cùng số electron nhưng khác nhau về tổng số proton và neutron.
-
Câu 17:
Thông tin nào sau đây không đúng về \({}_{{\rm{82}}}^{{\rm{206}}}{\rm{Pb}}\) ?
A. Số đơn vị điện tích hạt nhân là 82.
B. Số proton và neutron là 82.
C. Số neutron là 124.
D. ố khối là 206.
-
Câu 18:
Nhận định nào không đúng? Hai nguyên tử \({}_{{\rm{29}}}^{{\rm{63}}}{\rm{Cu}}\) và \({}_{{\rm{29}}}^{{\rm{65}}}{\rm{Cu}}\)
A. là đồng vị của nhau.
B. có cùng số electron.
C. có cùng số neutron.
D. có cùng số hiệu nguyên tử.
-
Câu 19:
Số electron tối đa ở lớp thứ n (n ≤ 4) là
A. n.
B. 2n.
C. 2n2.
D. n2.
-
Câu 20:
Nguyên tử nào sau đây có 3 electron ở lớp ngoài cùng?
A. N (Z = 7).
B. Na (Z = 11).
C. Al (Z = 13).
D. C (Z = 6).
-
Câu 21:
Hầu hết các chu kì trong bảng tuần hoàn các nguyên tố hóa học đều bắt đầu bằng
A. kim loại kiềm thổ.
B. kim loại kiềm.
C. halogen.
D. khí hiếm.
-
Câu 22:
Bảng tuần hoàn hiện nay có số cột là
A. 8
B. 16
C. 9
D. 18
-
Câu 23:
Các nguyên tố thuộc cùng một nhóm A trong bảng tuần hoàn sẽ có cùng
A. số electron hóa trị.
B. số hiệu nguyên tử.
C. số lớp electron.
D. số khối.
-
Câu 24:
Hình ảnh dưới đây là hình dạng của những loại orbital nguyên tử nào?
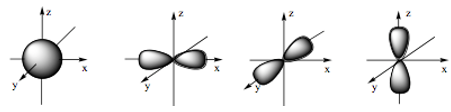
A. s, d.
B. d, f.
C. s, p.
D. p, f.
-
Câu 25:
Nguyên tử khối trung bình của nguyên tố X là 35,48. Biết trong tự nhiên, X có hai đồng vị, trong đó đồng vị 35X chiếm 75,77% số nguyên tử. Số khối của đồng vị còn lại là
A. 36
B. 37
C. 38
D. 39
-
Câu 26:
Chọn đáp án đúng. Orbital nguyên tử là
A. khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron là nhỏ nhất.
B. khu vực không gian xung quanh nguyên tử mà tại đó xác suất có mặt electron là lớn nhất.
C. khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron khoảng 90%.
D. quỹ đạo chuyển động của electron quay quanh hạt nhân có kích thước năng lượng xác định.
-
Câu 27:
Orbital s có dạng
A. hình elip.
B. hình cầu.
C. hình số tám nổi.
D. hình bầu dục.
-
Câu 28:
Số electron tối đa trong phân lớp 3p là
A. 8
B. 6
C. 3
D. 2
-
Câu 29:
Cấu hình electron nguyên tử nitrogen (Z = 7) là
A. 1s22s22p3.
B. 1s22s32p4.
C. 1s22s22p4.
D. 1s12s12p5.
-
Câu 30:
Lớp M có số electron tối đa bằng
A. 3
B. 4
C. 9
D. 18
-
Câu 31:
Cho cấu hình electron nguyên tử của các nguyên tố sau:
X: 1s22s22p63s2;
Y: 1s22s22p63s23p64s1;
Z: 1s22s22p63s23p3;
T: 1s22s22p63s23p63d84s2.
Các nguyên tử của nguyên tố kim loại là
A. X, Y, Z.
B. X, Y, T.
C. Y, Z, T.
D. X, Z, T.
-
Câu 32:
Mendeleev đã xây dựng bảng tuần hoàn bằng cách sắp xếp các nguyên tố theo chiều tăng dần của
A. số khối.
B. số hiệu nguyên tử.
C. khối lượng nguyên tử.
D. bán kính nguyên tử.
-
Câu 33:
Trong bảng hệ thống tuần hoàn, chu kì là dãy các nguyên tố mà
A. nguyên tử của chúng có cùng số electron lớp vỏ ngoài cùng.
B. cấu hình electron giống hệt nhau.
C. nguyên tử của chúng có cùng số lớp electron.
D. cấu hình electron lớp vỏ giống hệt nhau.
-
Câu 34:
Trong bảng hệ thống tuần hoàn các nguyên tố hóa học hiện nay, số chu kì nhỏ và chu kì lớn là
A. 3 và 3.
B. 3 và 4.
C. 4 và 3.
D. 4 và 4.
-
Câu 35:
Đặc điểm của hạt electron là
A. mang điện tích dương và có khối lượng.
B. mang điện tích âm và có khối lượng.
C. không mang điện và có khối lượng.
D. mang điện tích âm và không có khối lượng.
-
Câu 36:
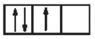
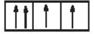
Sự phân bố electron theo ô orbital nào dưới đây là đúng?
A.
B.
C.
D.
-
Câu 37:
Cho biết cấu hình electron nguyên tử của các nguyên tố X: 1s22s22p63s2; Y: 1s22s22p63s23p64s1; Z: 1s22s22p63s23p5. Nguyên tố nào là kim loại?
A. X.
B. Z.
C. X và Y.
D. Y.
-
Câu 38:
Nguyên tử nguyên tố X có tổng các electron trên phân lớp p là 9. Vậy X thuộc loại nguyên tố nào sau đây?
A. s
B. d
C. f
D. p
-
Câu 39:
Trong bảng tuần hoàn, nguyên tố chlorine (kí hiệu: Cl) nằm ở chu kì 3, nhóm VIIA. Cấu hình electron của Cl là
A. 1s22s22p5.
B. 1s22s22p63s23p5.
C. 1s22s22p63s2.
D. 1s22s22p63s23p3.
-
Câu 40:
Nguyên tố X có cấu hình electron 1s22s22p63s23p64s1 thuộc
A. ô 19, chu kì 4, nhóm IA.
B. ô 19, chu kì 4, nhóm IB.
C. ô 19, chu kì 3, nhóm IVA.
D. ô 19, chu kì 3, nhóm IA.