Đề thi giữa HK1 môn Hóa học 11 năm 2022-2023
Trường THPT Lê Quý Đôn
-
Câu 1:
Dung dịch HNO3 đặc để lâu thường có màu vàng do
A. HNO3 tan nhiều trong nước.
B. HNO3 bị khử bởi các chất của môi trường
C. dung dịch HNO3 có tính oxi hóa mạnh.
D. dung dịch HNO3 có hoà tan một lượng nhỏ NO2.
-
Câu 2:
Trong phân tử H3PO4 photpho có số oxi hóa là
A. +5.
B. +3.
C. -5.
D. -3.
-
Câu 3:
Thuốc thử để phân biệt hai dung dịch Na3PO4 và NaNO3 là
A. AgNO3.
B. NaOH.
C. KOH.
D. HCl.
-
Câu 4:
Ở nhiệt độ thường, nitơ khá trơ về mặt hóa học do
A. nitơ có bán kính nguyên tử nhỏ.
B. nitơ có độ âm điện lớn nhất trongnhóm.
C. phân tử nitơ có liên kết ba rất bền.
D. phân tử nitơ không phân cực.
-
Câu 5:
Cho phản ứng: 2NH3 + 3Cl2 ⇌ 6HCl +N2. Kết luận nào sau đây đúng?
A. NH3 là chất khử.
B. NH3 là chất oxi hoá.
C. Cl2 vừa oxi hoá vừa khử.
D. Cl2 là chất khử.
-
Câu 6:
Ở 3000°C (hoặc có tia lửa điện) N2 hoá hợp với O2 theo phương trình phản ứng nào sau đây
A. N2 + O2 ⇌ 2NO.
B. N2 + 2O2 ⇌ 2NO2.
C. 4N2 + O2 ⇌ 2N2O.
D. 4N2 + 3O2 ⇌ 2N2O.
-
Câu 7:
Magie photphua có công thức là
A. Mg2P2O7.
B. Mg3P2.
C. Mg2P3.
D. Mg3(PO4)3.
-
Câu 8:
Từ 34 tấn NH3 sản xuất được 160 tấn dung dịch HNO3 63%. Hiệu suất
A. 80%
B. 50%
C. 60%
D. 85%.
-
Câu 9:
Xác định chất (A) và (B) trong chuỗi sau
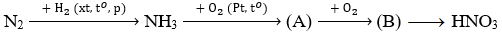
A. (A) là NO, (B) là N2O5.
B. (A) là N2, (B) là N2O5.
C. (A) là NO, (B) là NO2.
D. (A) là N2, (B) là NO2.
-
Câu 10:
Trong thí nghiệm đồng tác dụng với dung dịch HNO3 đặc để tránh khí độc NO2 bay ra người ta thường nút ống nghiệm bằng bông có tẩm dung dịch nào sau đây?
A. dd NaCl .
B. dd NaOH.
C. dd HCl.
D. dd NaNO3.
-
Câu 11:
Các số oxi hoá có thể có của photpho là
A. –3, +3, +5.
B. –3, +3, +5, 0.
C. +3, +5, 0.
D. –3, 0, +1, +3, +5.
-
Câu 12:
Cho các phản ứng: N2 + O2 ⇌ 2NO và N2 + 3H2 ⇌ 2NH3. Trong hai phản ứng trên thì nitơ
A. chỉ thể hiện tính oxi hóa.
B. chỉ thể hiện tính khử.
C. thể hiện cả tính khử và tính oxi hóa.
D. không thể hiện tính khử và tính oxi hóa.
-
Câu 13:
Khi cho kim loại Cu phản ứng với HNO3 tạo thành khí độc hại. Biện pháp nào xử lý tốt nhất để chống ô nhiễm môi trường?
A. Nút ống nghiệm bằng bông tẩm nước.
B. Nút ống nghiệm bằng bông tẩm cồn.
C. Nút ống nghiệm bằng bông tẩm giấm.
D. Nút ống nghiệm bằng bông tẩm nước vôi.
-
Câu 14:
Khi đốt cháy photpho trong khí Cl2 dư thì sản phẩm thu được là
A. PCl3.
B. PCl5.
C. PCl6.
D. PCl.
-
Câu 15:
Có thể dùng bình đựng HNO3 đặc, nguội bằng kim loại nào?
A. Đồng, bạc.
B. Đồng, chì.
C. Sắt, nhôm.
D. Đồng, kẽm.
-
Câu 16:
Cho các dung dịch: (NH4)2SO4; NH4Cl; Al(NO3)3; Fe(NO3)3; Cu(NO3)2 .Để phân biệt các dung dịch trên chỉ dùng 1 hóa chất nào sau?
A. Dung dịch NH3.
B. Dung dịch Ba(OH)2.
C. Dung dịch KOH.
D. Dung dịch NaCl.
-
Câu 17:
Chọn cấu hình electron lớp ngoài cùng của nguyên tố nhóm VA?
A. ns2np5.
B. ns2np3.
C. ns2np2.
D. ns2np4.
-
Câu 18:
Trong phản ứng nào sau đây, nitơ thể hiện tính khử?
A. N2 + 3H2 ⇌ 2NH3
B. N2 + 6Li → 2Li3N
C. N2 + O2 ⇌ 2NO
D. N2 + 3Mg → Mg3N2
-
Câu 19:
Cho sơ đồ sau

Trong sơ đồ A ,B lần lượt là các chất
A. HCl , HNO3
B. CaCl2 , HNO3
C. BaCl2 , AgNO3
D. HCl , NaNO3.
-
Câu 20:
Hiện tượng xảy ra khi cho giấy quỳ khô vào bình đựng khí amoniac là
A. Giấy quỳ chuyển sang màu đỏ.
B. Giấy quỳ chuyển sang màu xanh.
C. Giấy quỳ mất màu.
D. Giấy quỳ không chuyển màu.
-
Câu 21:
Nồng độ ion NO3- trong nước uống tối đa cho phép là 9 ppm. Nếu thừa ion NO3- sẽ gây một loại bệnh thiếu máu hoặc tạo thành nitrosamin, một hợp chất gây ung thư đường tiêu hóa. Để nhận biết ion NO3-, người ta dùng
A. CuSO4 và NaOH.
B. Cu và NaOH.
C. Cu và H2SO4.
D. CuSO4 và H2SO4.
-
Câu 22:
Nhiệt phân hoàn toàn Fe(NO3)2 trong không khí thu được sản phẩm gồm
A. FeO, NO2, O2.
B. Fe2O3, NO2.
C. Fe2O3, NO2, O2.
D. Fe, NO2, O2.
-
Câu 23:
Dãy gồm tất cả các chất khi tác dụng với HNO3 thì HNO3 chỉ thể hiện tính axit là
A. CaCO3, Cu(OH)2, Fe(OH)2, FeO.
B. CuO, NaOH, FeCO3, Fe2O3.
C. Fe(OH)3, Na2CO3, Fe2O3, NH3.
D. KOH, FeS, K2CO3, Cu(OH)2.
-
Câu 24:
Thuốc thử dùng để phân biệt ba dung dịch muối NaNO3, Na3PO4, NaCl là
A. AgNO3.
B. BaCl2.
C. NaOH.
D. H2SO4.
-
Câu 25:
Khi nhiệt phân AgNO3 thu được những sản phẩm nào?
A. Ag, NO2, O2.
B. Ag, NO,O2.
C. Ag2O, NO2, O2.
D. Ag2O, NO, O2.
-
Câu 26:
Trộn 100 ml dung dịch NaOH 0,15M với 100 ml dung dịch H3PO4 0,1M thì thu được dung dịch X gồm
A. Na2HPO4 và NaH2PO4.
B. Na3PO4 và Na2HPO4.
C. Na3PO4 và NH2PO4.
D. Na3PO4 và NaOHdư.
-
Câu 27:
Hòa tan 32 g hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư), thoát ra 6,72 lít khí NO (đktc). Khối lượng CuO trong hỗn hợp ban đầu là
A. 1,2g.
B. 1,88g.
C. 2,52g.
D. 3,2g.
-
Câu 28:
Chọn phát biểu đúng?
A. Photpho trắng tan trong nước không độc.
B. Photpho trắng được bảo quản bằng cách ngâm trong nước.
C. Photpho trắng hoạt động hoá học kém hơn photpho đỏ.
D. Photpho đỏ phát quang màu lục nhạt trong bóng tối.
-
Câu 29:
Cho m(g) Al tan hoàn toàn trong dung dịch HNO3 thấy tạo ra 11,2 lít (đktc) hỗn hợp 3 khí NO, N2O, N2 với tỷ lệ mol tương ứng là 1: 2 : 2. Giá trị của m là
A. 16.47g.
B. 23g.
C. 35.1g.
D. 12.73g.
-
Câu 30:
Hòa tan hết m(g) Al trong dung dịch HNO3, thu được hỗn hợp khí (đktc) gồm NO và NO2 có thể tích là 8,96 lít và có tỷ khối đối với hiđro là 16,75. Giá trị của m là
A. 9,252.
B. 2,7g.
C. 8,1g.
D. 9,225g.
-
Câu 31:
Hoà tan hoàn toàn 19,2 gam một kim loại M trong dung dịch HNO3 ta thu được 4,48 lít NO (đktc). Kim loại M là
A. Zn (M = 65).
B. Fe (M = 56).
C. Mg (M = 24).
D. Cu (M = 64).
-
Câu 32:
Cho 39 gam kim loại M phản ứng hoàn toàn với dung dịch HNO3 thu được 8,96 lit khí NO (là sản phẩm khử duy nhất ở đktc). Kim loại M là
A. Zn.
B. Ca.
C. Cu.
D. Mg.
-
Câu 33:
Nitơ đóng vai trò là chất oxi hóa trong phản ứng với
A. oxi và các chất oxi hóa khác.
B. hiđro và oxi.
C. kim loại và oxi.
D. kim loại và hiđro.
-
Câu 34:
Cho 9,6 gam Cu tác dụng hết với dd HNO3 loãng. Thể tích khí NO là sản phẩm khử duy nhất ở đktc thu được là
A. 3,36 lít.
B. 2,24 lít.
C. 4,48 lít.
D. 6,72 lít.
-
Câu 35:
Cho dung dịch KOH dư vào 150ml dd NH4Cl 1M. Đun nhẹ thu được thể tích khí thoát ra ở (đktc) là
A. 2,24 lit.
B. 3,36 lit.
C. 1,12 lit.
D. 4.48 lit.
-
Câu 36:
Để điều chế 4 lít NH3 từ N2 và H2 với hiệu suất 25% thì thể tích N2 cần dùng ở cùng điều kiện là
A. 8 lít.
B. 16 lít.
C. 2 lít.
D. 4 lít.
-
Câu 37:
Hòa tan hoàn toàn 15,9g hỗn hợp 3 kim loại Al, Mg, Cu bằng dd HNO3 thu được 6,72 lit khí NO (là sản phẩm khử duy nhất ở đktc) và dd X. Đem cô cạn dd X thì thu được khối lượng muối khan là
A. 77,1g.
B. 71,7g.
C. 17,7g.
D. 53,1g.
-
Câu 38:
Hòa tan hoàn toàn 6,4 gam kim loại R có hóa trị II trong dung dịch HNO3 dư thu được 4,48 lít khí NO2 (đktc) là sản phẩm khử duy nhất. Kim loại R là (Cho: Zn = 65, Cu = 64, Al = 27, Fe = 56)
A. Zn.
B. Cu.
C. Al.
D. Fe.
-
Câu 39:
Cho 1,92 gam Cu vào 100ml dung dịch chứa đồng thời KNO3 0,16M và H2SO4 0,4M thấy sinh ra một chất khí có tỉ khối so với H2 là 15 và dung dịch A. Thể tích khí sinh ra (ở đktc) là
A. 3,584 lít.
B. 0,3584lít.
C. 35,84 lít.
D. 358,4 lít.
-
Câu 40:
Thực hiện phản ứng giữa H2 và N2 trong bình kín có xúc tác thu được 1,7 gam NH3 với hiệu suất phản ứng là 80%. Thể tích H2 (đktc) cần dùng cho phản ứng là (Cho: N = 14, H = 1)
A. 4,2 lít.
B. 2,4 lít.
C. 4 lít.
D. 5lít.











