Đề thi HK1 môn Hóa 11 năm 2022-2023
Trường THPT Nguyễn Du
-
Câu 1:
Phương trình ion: OH- + HCO3-→ CO32- + H2O là của phản ứng xảy ra giữa cặp chất nào sau đây?
A. NaOH + Ba(HCO3)2.
B. Ba(HCO3)2 + Ba(OH).
C. NaHCO3 + Ba(OH)2
D. NaHCO3 + NaOH.
-
Câu 2:
Kim loại bị thụ động trong HNO3 đặc, nguội là
A. Pt, Cu.
B. Al, Fe.
C. Ag, Fe.
D. Pb, Ag.
-
Câu 3:
Nồng độ mol của anion trong dung dịch BaCl2 0,20M là
A. 0,40M.
B. 0,20M
C. 0,30M.
D. 0,10M.
-
Câu 4:
Cho P tác dụng với Mg, sản phẩm thu được là
A. Mg2P2O7.
B. Mg3P2.
C. Mg(PO3)2.
D. Mg3(PO4)2.
-
Câu 5:
Trong những nhận xét dưới đây về muối amoni, nhận xét nào là đúng?
A. Muối amoni là tinh thể ion, phân tử gồm cation amoni và anion hiđroxit.
B. Tất cả các muối amoni đều dễ tan trong nước, khi tan điện li hòa toàn thành cation amoni và anion gốc axit.
C. Dung dịch muối amoni tác dụng với dung dịch kiềm đặc, nóng cho thoát ra chất khí làm quỳ tím hóa đỏ.
D. Khi nhiệt phân muối amoni luôn luôn có khí amoniac thoát ra.
-
Câu 6:
Chất phản ứng được với NH3 là
A. Na2O.
B. AlCl3 (dd).
C. Na2CO3 (dd).
D. NaOH (dd).
-
Câu 7:
Các nguyên tử thuộc nhóm IVA có cấu hình electron lớp ngoài cùng là
A. ns2np5.
B. ns2np3.
C. ns2np4.
D. ns2np2.
-
Câu 8:
Khí amoniac làm giấy quỳ tím ẩm
A. chuyển thành màu xanh.
B. mất màu.
C. chuyển thành màu đỏ
D. không đổi màu.
-
Câu 9:
Chất khí nào sau đây được tạo ra từ bình chữa cháy và dùng để sản xuất đá khô?
A. H2O.
B. N2.
C. CO2.
D. CO.
-
Câu 10:
Dung dịch KOH 0,001M cần pha loãng bằng nước bao nhiều lần để được dung dịch có pH = 9?
A. 80 lần
B. 90 lần
C. 100 lần
D. 110 lần
-
Câu 11:
Biết độ điện li của dung dịch axit CH3COOH 1,2M là 1,5%. Nồng độ mol/l của ion CH3COO- trong dung dịch trên là
A. 0,018M
B. 0,015M
C. 0,012 M
D. 0,014M.
-
Câu 12:
Cho 1,92 gam Cu tác dụng vừa hết với V lít dung dịch HNO3 0,1M loãng giải phóng khí NO. Giá trị của V là
A. 0,80 lít
B. 0,85 lít
C. 0,90 lít.
D. 0,95 lít.
-
Câu 13:
Cho 0,15 mol hỗn hợp NaHCO3 và MgCO3 tác dụng hết với dung dịch HCl. Khí thoát ra được dẫn vào dung dịch Ca(OH)2 dư thu được kết tủa có khối lượng là
A. 8 gam
B. 15 gam
C. 20 gam
D. 34 gam.
-
Câu 14:
Dãy gồm các ion cùng tồn tại trong một dung dịch là
A. K+, Ba2+, OH- , Cl- .
B. Mg2+, Ba2+, Cl- ,CO32- .
C. Na+, K+, OH- , HCO3- .
D. Na+, Ag+ , NO3- ,Cl- .
-
Câu 15:
Phản ứng hóa học, trong đó cacbon có tính khử là
A. 2C + Ca → CaC2
B. C + 2H2 → CH4
C. C + CO2 → 2CO
D. 3C + 4Al → Al4C3
-
Câu 16:
Các hình vẽ sau mô tả các cách thu khí trong phòng thí nghiệm:
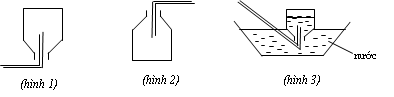
Kết luận nào sau đây đúng?
A. Hình 3: Thu khí N2, H2 và HCl.
B. Hình 2: Thu khí CO2, SO2 và NH3.
C. Hình 3: Thu khí N2, H2 và NH3.
D. Hình 1: Thu khí H2, He và NH3.
-
Câu 17:
Khi nhiệt phân, dãy muối rắn nào dưới đây đều sinh ra kim loại, khí nitơ đioxit và oxi?
A. AgNO3, Hg(NO3)2.
B. Cu(NO3)2, Mg(NO3)2.
C. Hg(NO3)2, Mg(NO3)2.
D. AgNO3, Cu(NO3)2.
-
Câu 18:
Độ dinh dưỡng của phân lân được tính bằng
A. % P2O5.
B. % P.
C. % PO43-.
D. Ca(H2PO4)2.
-
Câu 19:
Chất nào sau đây thuộc loại chất điện li yếu?
A. H2SO4.
B. KOH.
C. CH3COOH.
D. NaCl.
-
Câu 20:
Cho dung dịch KOH đến dư vào 50 ml (NH4)2SO4 1M. Đun nóng nhẹ, thu được thể tích khí thoát ra (đktc) là
A. 1,12 lít
B. 4,48 lít.
C. 0,112 lít.
D. 2,24 lít.
-
Câu 21:
Sục 0,15 mol khí CO2 vào 200 ml dung dịch Ba(OH)2 1M, kết thúc phản ứng thu được các chất
A. Ba(HCO3)2 và Ba(OH)2 dư.
B. Ba(HCO3)2.
C. Ba(HCO3)2 và BaCO3.
D. BaCO3, Ba(OH)2 dư.
-
Câu 22:
Số liên kết xích-ma (Ϭ) trong phân tử C4H10 là
A. 10
B. 13
C. 12
D. 14
-
Câu 23:
Cặp chất nào dưới đây là dồng phân của nhau?
A. CH3CH2CH2OH, CH3OCH2CH3
B. CH3OCH3, CH3CHO
C. CH3OH, C2H5OH
D. CH3CH2OH, CH3CH2Br
-
Câu 24:
Chất nào sau đây là dẫn xuất của hiđrocacbon?
A. CH4
B. C2H6
C. C6H6
D. C3H6Br.
-
Câu 25:
Cho các hợp chất: C2H6; C2H2; C2H4O2; C2H6O; C6H12O6. Hợp chất nào sau đây có hàm lượng cacbon cao nhất?
A. C2H6
B. C2H2
C. C6H12O6
D. C2H4O2
-
Câu 26:
Đốt cháy hoàn toàn một hiđrocacbon (X) thu được \({{n_{C{O_2}}} = \frac{1}{2}{n_{{H_2}O}}}\) . Vậy X là:
A. C2H6
B. C3H6
C. CH4
D. C2H4
-
Câu 27:
Khí nitơ có thể được tạo thành trong phản ứng hóa học nào sau đây?
A. Đốt cháy NH3 trong oxi có mặt chất xúc tác platin.
B. Nhiệt phân NH4NO2.
C. Nhiệt phân AgNO3.
D. Nhiệt phân NH4NO3.
-
Câu 28:
Chất nào sau đây có tên gọi là amoni hiđrosunfat?
A. NH4HSO4.
B. (NH4)2SO4
C. NH4HCO3.
D. NH4SO4
-
Câu 29:
Trong công nghiệp, nitơ điều chế bằng cách:
A. dùng than nóng đỏ tác dụng hết với không khí ở nhiệt độ cao.
B. dùng đồng để oxi hoá hết oxi của không khí ở nhiệt độ cao.
C. hoá lỏng không khí và chưng cất phân đoạn.
D. dùng H2 tác dụng hết oxi không khí ở nhiệt độ cao rồi ngưng tụ hơi nước.
-
Câu 30:
Cho dung dịch NH3 dư vào dung dịch nhôm sunfat thì
A. xuất hiện kết tủa rồi kết tủa tan do Al(OH)3 là hiđroxit lưỡng tính.
B. xuất hiện kết tủa rồi kết tủa tan do tạo phức.
C. xuất hiện kết tủa không tan trong dung dịch NH3 dư.
D. xuất hiện kết tủa và có khí không màu không mùi thoát ra.
-
Câu 31:
Cho 0,05 mol Mg tan hết trong dung dịch HNO3 thấy thoát ra 0,01 mol khí X là sản phẩm khử duy nhất (đktc). X là
A. NO2.
B. N2.
C. NO.
D. N2O.
-
Câu 32:
Nhiệt phân hoàn toàn 18,9 gam muối nitrat của một kim loại hóa trị II, thu được 5,6 lít hỗn hợp khí ở đktc. Kim loại đó là
A. Fe.
B. Fe.
C. Mg.
D. Zn.
-
Câu 33:
Sản phẩm của phản ứng nhiệt phân Cu(NO3)2 là
A. Cu(NO3)2, NO2 và O2.
B. CuO, NO và O2.
C. CuO, NO2 và O2.
D. Cu(NO2)2 và O2.
-
Câu 34:
Dãy chất nào sau đây, trong nước đều là chất điện li mạnh?
A. H3PO4, Fe(NO3)3.
B. MgCl2, Ba(OH)2.
C. CH3COOH, BaCl2.
D. H2SO4, H2S.
-
Câu 35:
Nồng độ mol của cation trong dung dịch Ba(NO3)2 0,45M là
A. 0,45M.
B. 1,35M.
C. 1,00M.
D. 0,90M.
-
Câu 36:
Cặp chất nào sau đây là đồng đẳng của nhau?
A. CH3OH, CH3OCH3.
B. CH3OCH3, CH3CHO.
C. CH3OH, C2H5OH.
D. CH3CH2OH, C3H6(OH)2.
-
Câu 37:
Số công thức cấu tạo mạch hở ứng với các công thức phân tử C2H6O là
A. 3
B. 2
C. 1
D. 4
-
Câu 38:
N2 thể hiện tính khử trong phản ứng với
A. Li.
B. H2
C. Mg.
D. O2.
-
Câu 39:
Thể tích của 1,5 gam chất X bằng thể tích của 0,8 gam khí oxi (đktc cùng điều kiện nhiệt độ, áp suất). Phân tử khối của X là
A. 60
B. 30
C. 120
D. 32.
-
Câu 40:
Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X (C, H, O) thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O. Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của X là
A. C5H12O
B. C2H4O
C. C3H4O3
D. C4H8O2.











