Trắc nghiệm Điều chế kim loại Hóa Học Lớp 12
-
Câu 1:
Có thể dùng phương pháp nào để điều chế được tất cả kim loại : Mg ,Ba, K
-
Câu 2:
Để điều chế Fe trong công nghiệp, người ta có thể dùng phương pháp nào sau đây:
-
Câu 3:
Để điều chế Al kim loại ta có thể dùng phương pháp nào trong các phương pháp sau đây
-
Câu 4:
Chất nào sau đây được điều chế trong công nghiệp bằng phương pháp điện phân?
-
Câu 5:
Tiến hành ĐP 100 ml CuSO4 0,2 M với cường độ dòng điện 9,65A. Tính khối lượng Cu bám vào catot khi thời gian điện phân t1 = 200 s và t2 = 500 s. Biết hiệu suất điện phân là 100 %
-
Câu 6:
Điện phân chất X gồm 0,1 mol CuSO4 và 0,1 mol KCl. Khi ở catot bắt đầu thoát khí thì ngừng điện phân. Khối lượng kim loại trên catot và thể tích khí thu được ở anot (đktc) lần lượt là gì?
-
Câu 7:
Tiến hành điện phân 200 ml hỗn hợp AgNO3 0,1 M và Cu(NO3)2 0,2 M với điện cực trơ và I = 5A. Sau 19 phút 18 giây dừng điện phân, lấy catot sấy khô thấy tăng m gam. Giá trị của m là:
-
Câu 8:
Tiến hành điện phân 100 ml hỗn hợp gồm FeCl3 1M , FeCl2 2M , CuCl2 1M và HCl 2M với điện cực trơ có màng ngăn xốp cường độ dòng điện là 5A trong 2 giờ 40 phút 50 giây ở catot thu được?
-
Câu 9:
Điện phân 500 ml NaCl 1M điện cực trơ, màng ngăn xốp cho tới khi catot thoát ra 0,56 lít khí X (đktc) thì ngưng điện phân. Nếu coi thể tích dung dịch sau điện phân không thay đổi so với ban đầu thì giá trị pH của dung dịch này là?
-
Câu 10:
Điện phân 500 ml CuSO4 0,2M (điện cực trơ) cho đến khi catot thu được 3,2 gam kim loại thì thể tích khí (đktc) thu được ở anot là?
-
Câu 11:
Điện phân hỗn hợp gồm 0,1 mol FeCl3, 0,2 mol CuCl2 và 0,1 mol HCl (điện cực trơ). Khi ở catot bắt đầu thoát khí thì ở anot thu được V lít khí (đktc). Biết hiệu suất của quá trình điện phân là 100%. Giá trị của V là bao nhiêu?
-
Câu 12:
Điện phân 100 ml Fe(NO3)3 1M và Cu(NO3)2 1M trong bình điện phân với điện cực trơ, I =19,3A, sau một thời gian lấy catot ra cân lại thấy nó nặng thêm 3,584 gam (giả thiết rằng toàn bộ kim loại sinh ra đều bám vào catot). Tính thời gian điện phân?
-
Câu 13:
Tiến hành điện phân điện cực trơ V lít CuCl2 0,5M. Khi dừng điện phân thu được dung dịch X và 1,68 lít khí Cl2 (đktc) duy nhất ở anot. Toàn bộ dung dịch X tác dụng vừa đủ với 12,6 gam Fe. Giá trị của V là gì?
-
Câu 14:
Điện phân muối nitrat của một kim loại M, đến khi thấy thoát ra 2,24 lít khí (đktc) ở anot thì ở catot có 43,2 g kim loại. Tìm công thức của muối biết không có khí thoát ra ở catot.
-
Câu 15:
Điện phân 150 ml AgNO3 1M với điện cực trơ trong t giờ, cường độ dòng điện không đổi 2,68A (hiệu suất quá trình điện phân là 100%), thu được chất rắn X, dd Y và khí Z. Cho 12,6 gam Fe vào Y, sau khi các phản ứng kết thúc thu được 14,5 gam hỗn hợp kim loại và khí NO (sản phẩm khử duy nhất của N+5). Giá trị của t là?
-
Câu 16:
Nếu muốn điện phân hoàn toàn 400 ml dung dịch CuSO4 0,5M với cường độ dòng điện I = 1,34A (hiệu suất điện phân là 100%) thì mất bao lâu?
-
Câu 17:
Điện phân CuSO4 dư trong thời gian 1930 giây, thu được 1,92 gam Cu ở catot, hãy xác định cường độ dòng điện?
-
Câu 18:
Điện phân CuCl2 bằng I = 5A trong 45 phút 20 giây. Tính khối lượng kim loại sinh ra ở Catot ?
-
Câu 19:
Điện phân 2,22 gam muối clorua nào bên dưới đây để thu được 448 ml khí (ở đktc) ở anot.
-
Câu 20:
Điện phân MCln với điện cực trơ ở catot thu 16g kim loại M thì ở anot thu được 5,6 lít khí (đktc). Từ đây hãy xác định tên kim loại?
-
Câu 21:
Điện phân 1,9g muối clorua của kim loại M được 0,48g kim loại nào ở catot.
-
Câu 22:
Điện phân MgCl2 (điện cực trơ, có màng ngăn xốp bao điện cực) với cường độ dòng điện 2,68A trong 2 giờ. Sau khi dừng điện phân khối lượng dung dịch giảm bao nhiêu gam?
-
Câu 23:
Khi điện phân thì các muối X- (X: Cl-, Br-) di chuyển về đâu?
-
Câu 24:
Thể tích khí (đktc) thoát ra ở anot sau 26055 giây khi điện phân 0,2 mol CuSO4; 0,12 mol Fe2(SO4)3 và 0,44 mol NaCl bằng dòng điện có cường độ 2 ampe?
-
Câu 25:
Điện phân CuCl2 bằng dòng điện 5A trong 45 phút 20 giây hãy tính khối lượng kim loại sinh ra trên catot và thể tích khí sinh ra ở anot?
-
Câu 26:
Điện phân muối MCln với điện cực trơ. Khi ở catot thu được 16g kim loại nào sau đây thì ở anot thu được 5,6 lít khí (đktc).
-
Câu 27:
Có 400ml dung dịch chứa HCl và KCl với nồng độ mol/lit là bao nhiêu biết đem điện phân trong bình điện phân có vách ngăn với cường độ dòng điện 9,65A trong 20 phút thì dung dịch chứa một chất tan có pH = 13?
-
Câu 28:
Điện Cu(NO3)2 với I = 9,65A đến khi bắt đầu có khí thoát ra ở catot thì dừng lại. thời gian điện phân là 40 phút hãy tính mCu sinh ra?
-
Câu 29:
Điện phân 18,8g Cu(NO3)2 và 29,8g KCl thì khối lượng dung dịch giảm 17,15g so với ban đầu, thể tích dung dịch là 400ml. Nồng độ mol lớn nhất của các chất sau điện phân?
-
Câu 30:
Hãy tìm X, Y, Z và T thõa mãn:
Chất
Cách làm
X
Y
Z
T
Thí nghiệm 1: Thêm dung dịch NaOH (dư)
Có kết tủa sau đó tan dần
Có kết tủa sau đó tan dần
Có kết tủa không tan
Không có kết tủa
Thí nghiệm 2: Thêm tiếp nước brom vào các dung dịch thu được ở thí nghiệm 1
Không có hiện tượng
Dung dịch chuyển sang màu vàng
Không có hiện tượng
Không có hiện tượng
-
Câu 31:
Trong hình vẽ sau chi tiết nào chưa đúng khi cắm hai lá Cu và Zn (được nối với nhau bằng một dây dẫn) vào dung dịch H2SO4 loãng?
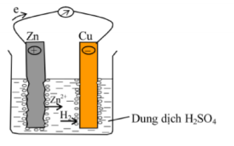
-
Câu 32:
Điện phân 200ml NaCl 2M (d = 1,1g/ml) với điện cực C có màng ngăn xốp khí ở catot thoát ra 22,4 lít khí đo ở điều kiện tiêu chuẩn thì ngừng điện phân. Hãy tính nồng độ phần trăm của dung dịch NaOH?
-
Câu 33:
Điện phân 200 ml dung dịch CuSO4 (d = 1,25 g/ml) với điện cực graphit (than chì) thấy khối lượng dung dịch giảm 8 gam sau 1 thời gian. Để làm kết tủa hết ion Cu2+ còn lại sau điện phân cần dùng 100 ml dung dịch H2S 0,5 M. Tính C% dung dịch CuSO4 ?
-
Câu 34:
Điện phân dung dịch chứa 0,2 mol NaCl và x mol Cu(NO3)2 (điện cực trơ,màng ngăn xốp) sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn thấy khối lượng thanh sắt giảm 2,6 gam và thấy thoát ra khí NO duy nhất. Giá trị của x là
-
Câu 35:
Cho một dòng điện có cường độ không đổi đi qua 2 bình điện phân mắc nối tiếp. Bình 1 chứa 500 ml dung dịch CuSO4 (điện cực trơ), bình 2 chứa 100 ml dung dịch hỗn hợp AgNO3 0,2M; Cu(NO3)2 0,3M, Fe(NO3)3 0,1M (điện cực trơ). Sau một thời gian ngắt dòng điện, thấy bình 1 có pH =1 và catot của bình 2 tăng thêm m gam. Biết thể tích dung dịch không thay đổi trong suốt quá trình điện phân. Giá trị của m là
-
Câu 36:
Điện phân dung dịch hỗn hợp CuSO4 và KCl với điện cực trơ, có màng ngăn xốp. Khi ở cả hai điện cực đều có bọt khí thì dừng lại. Kết quả ở anot có 448ml khí thoát ra (dktc), khối lượng dung dịch sau điện phân giảm m gam và dung dịch sau điện phân có thể hòa tan tối đa 0,8 gam MgO. Giá trị của m là :
-
Câu 37:
Điện phân (điện cực trơ, hiệu suất 100%) 300 ml dung dịch CuSO4 0,5M với cường độ dòng điện không đổi 2,68 A, trong thời gian t giờ thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X thấy xuất hiện 45,73 gam kết tủa. Giá trị của t là
-
Câu 38:
Điện phân 200 ml dung dịch muối CuSO4 trong thời gian, thấy khối lượng dung dịch giảm 8 gam. Dung dịch sau điện phân cho tác dụng với dd H2S dư thu được 9,6g kết tủa đen. Nồng độ mol của dung dịch CuSO4 ban đầu là
-
Câu 39:
Điện phân 500 ml dung dịch hỗn hợp gồm NaCl 0,1M và AlCl3 0,3M có màng ngăn, điện cực trơ tới khi ở anot bắt đầu xuất hiện khí thứ 2 thì ngừng điện phân. Sau điện phân, lọc lấy kết tủa rồi nung ở nhiệt độ cao đến khối lượng không đổi được m gam chất rắn. Giá trị của m là
-
Câu 40:
Điện phân hoàn toàn 200ml dung dịch AgNO3 với 2 điên cực trơ thu được một dung dịch có pH= 2. Xem thể tích dung dịch thay đổi không đáng kể thì lượng Ag bám ở catot là?
-
Câu 41:
Điện phân dd hh chứa 0,04mol AgNO3 và 0,05mol Cu(NO3)2 (điện cực trơ), dòng điện 5A, trong 32 phút 10 giây. Khối lượng kim loại bám vào catot là:
-
Câu 42:
Điện phân 200ml dd CuSO4 0,2M với cường độ dòng điện không đổi trong thời gian t giây thấy có 224ml khí (đktc) thoát ra ở anot. Biết điện cực trơ và hiệu suất phản ứng là 100%. Khối lượng kim loại bám ở catot là:
-
Câu 43:
Tiến hành điện phân V lít dung dịch NaCl 1M và CuSO4 1,8M bằng điện cực trơ tới khi nước bắt đầu điện phân ở cả hai cực thì dừng điện phân, thấy khối lượng dung dịch giảm m gam. Dung dịch sau phản ứng hòa tan tối đa 8,84 gam Al2O3. Giá trị của m là:
-
Câu 44:
Điện phân 100 ml dung dịch AgNO3 1M với các điện cực trơ, thời gian điện phân là 14 phút 15 giây, cường độ dòng điện không đổi là 0,8 A (H = 100%). Khối lượng catot tăng lên là:
-
Câu 45:
Điện phân một dd muối MCln với điện cực trơ. Khi ở catot thu được 16g kim loại M thì ở anot thu được 5,6 lít khí (đktc). Kim loại M là:
-
Câu 46:
Điện phân một lượng dư dung dịch MgCl2 (điện cực trơ, có màng ngăn xốp bao điện cực) với cường độ dòng điện 2,68A trong 2 giờ. Sau khi dừng điện phân khối lượng dung dịch giảm m gam, giả thiết nước không bay hơi, các chất tách ra đều khan. Giá trị của m là.
-
Câu 47:
Điện phân nóng chảy hoàn toàn 1,9g muối clorua của kim loại M được 0,48g kim loại M ở catot. Kim loại M là:
-
Câu 48:
Điện phân dung dịch chứa 23,4 gam muối ăn (với điện cực trơ, màng ngăn xốp), thu được 2,5 lít dung dịch có pH=13. Phần trăm muối ăn bị điện phân là
-
Câu 49:
Một học sinh thực hiện quá trình điện phân dung dịch chứa đồng thời CuSO4 và FeSO4 bằng hệ điện phân sử dụng các điện cực than chì, hãy cho biết: Bán phản ứng nào xảy ra ở anot?
-
Câu 50:
Điện phân dung dịch chứa a mol CuSO4 và b mol NaCl (với điện cực trơ, có màng ngăn xốp). Để dung dịch sau điện phân làm phenolphtalein chuyển sang màu hồng thì điều kiện của a và b là :











