Trắc nghiệm Tính chất Hóa học của Lưu huỳnh ddioxit và lưu huỳnh trioxit Hóa Học Lớp 10
-
Câu 1:
Thể tích dung dịch NaOH 2M tối thiểu để hấp thụ hết 5,6 lit khí SO2 (đkc) là bao nhiêu?
-
Câu 2:
Tính V khí SO2 (đktc) cần dùng khi cho vào 200 ml dung dịch Ba(OH)2 1M biết sau phản ứng thu được 21,7 gam kết tủa.
-
Câu 3:
Cho 6,72 lít khí SO2 (đkc) tác dụng với 180 ml dung dịch NaOH 2M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X. Tính khối lượng muối có trong dung dịch X?
-
Câu 4:
Dẫn 5,6 lít SO2 (đktc) vào 600 ml dung dịch NaOH 1M, sau phản ứng thu được dung dịch B Thêm BaCl dư vào dung dịch B thu được m gam kết tủa Giá trị của m là:
-
Câu 5:
V lít SO2 (đktc) + 500ml dung dịch Ca(OH)2 0,5M tạo thành 12 gam kết tủa. Tìm Vmax ?
-
Câu 6:
Hấp thụ hoàn toàn 2,688 lít khí SO2 (đktc) + 2,5 lít Ba(OH)2 nồng độ a M. Thu được 17,36 gam kết tủa. Giá trị của a?
-
Câu 7:
Tính m kết tủa thu được khi đốt cháy hoàn toàn 4,8 gam lưu huỳnh rồi cho sản phẩm cháy hấp thụ hoàn toàn vào 200 ml dung dịch Ba(OH)2 0,5M.
-
Câu 8:
Thể tích dung dịch NaOH 2M tối thiểu để hấp thụ hết 5,6 lit khí SO2 (đkc) là:
-
Câu 9:
Ở PTN, điều chế một lượng lớn SO2 (để thực hành thí nghiệm) ta dùng phản ứng có phương trình hóa học là?
-
Câu 10:
Nêu hiệu tượng khi SO2 tác dụng với H2S?
-
Câu 11:
Trong bình cầu xảy ra phản ứng nào?
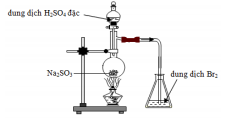
-
Câu 12:
Trong phòng thí nghiệm, khi tiến hành thí nghiệm cho mảnh đồng vào ống nghiệm của H2SO4 đặc, đun nóng thấy sinh ra chất khí SO2 có mùi hắc, độc. Biện pháp nào sau đây xử lí thoát ra chống ô nhiễm môi trường?
-
Câu 13:
Tính oxi hóa của SO2 thể hiện ở?
-
Câu 14:
Tại sao SO2 vừa có tính oxi hoá, vừa có tính khử?
-
Câu 15:
Dẫn khí SO2 vào lượng dư dung dịch Ca(OH)2, muối gì được tạo thành?
-
Câu 16:
Cho các phản ứng sau:
2SO2 + O2 → 2SO3 (I)
SO2 + 2H2S → 3S + 2H2O (II)
SO2 + Br2 + 2H2O → H2SO4 + 2HBr (III)
SO2 + NaOH → NaHSO3 (IV)
Các phản ứng mà SO2 có tính khử là:
-
Câu 17:
Từ phản ứng SO2 + 2H2S → 3S + 2H2O. Câu nào diễn tả đúng tính chất của các chất ?
-
Câu 18:
Dẫn từ từ đến dư SO2 vào dung dịch brom thì?
-
Câu 19:
Có 5 lọ không ghi nhãn đựng 5 hoá chất riêng rẽ gồm: KCl, K2CO3, Na2SO4, HCl, Ba(NO3)2 . Chỉ dùng giấy quỳ xanh có thể nhận ra:
-
Câu 20:
Để một ít vỏ bào hoặc mùn cưa (là những hợp chất gluxit) trong cốc thuỷ tinh, sau đó nhỏ từ từ H2SO4 đặc vào. Sẽ thấy vỏ bào hoặc mùn cưa biến thành màu đen và có bọt khí sủi lên. Giải thích hiện tượng này một cách đúng nhất là
-
Câu 21:
Khi cho từ từ muối CuSO4. 5H2O màu xanh vào ống nghiệm chứa H2SO4 98%, thì muối đồng chuyển dần sang màu trắng vì:
-
Câu 22:
Có những hoá chất Na2SO3, CaSO3, BaSO3, CuSO3 và dung dịch H2SO4. Những hoá chất có thể cho tác dụng với dung dịch H2SO4 để điều chế khí SO2 thuận lợi nhất là:
-
Câu 23:
Có 3 lọ đựng 3 chất khí riêng biệt là SO2, CO2, Cl2. Chỉ dùng dung dịch Br2 có thể phân biệt được mấy chất?
-
Câu 24:
Có 4 bình đựng 4 chất khí riêng biệt là O2, SO2, CO2, SO3. Chỉ dùng dung dịch Br2 thì có thể phân biệt được bình đựng khí:
-
Câu 25:
Trong công nghiệp luyện kim màu, người ta thu được lượng lớn sản phẩm phụ là SO2. Trong khí tự nhiên có lượng đáng kể khí H2S. Những khí này là nguyên nhân gây ô nhiễm môi trường không khí. Người ta đã thực hiện phương pháp sản xuất lưu huỳnh từ 2 chất khí trên để thu được đến 90% lưu huỳnh trong các chất độc loại đó. Phản ứng điều chế S là:
-
Câu 26:
Có các hoá chất sau: Na2SO3, CaSO3, PbSO3, BaSO3 và dung dịch H2SO4. Có thể điều chế SO2 trong phòng thí nghiệm bằng phản ứng:












