Đề thi giữa HK1 môn Hóa học 11 năm 2022-2023
Trường THPT Hai Bà Trưng
-
Câu 1:
Xác định chất A, B trong chuỗi sau:
A. A là NO, B là N2O5
B. A là NO, B là NO2
C. A là N2, B là N2O5
D. A là N2, B là NO2
-
Câu 2:
Phản ứng trao đổi ion trong dung dịch các chất điện li xảy ra khi
A. Tạo thành chất điện li yếu
B. Tạo thành chất khí
C. Tạo thành chất kết tủa
D. Có ít nhất 1 trong 3 điều kiện trên
-
Câu 3:
Để tạo độ xốp cho một số loại bánh, trong bột nở thường dùng loại muối nào sau đây
A. (NH4)2SO4
B. CaCO3
C. NH4NO2
D. NH4HCO3
-
Câu 4:
Dãy gồm các ion có thể cùng tồn tại trong một dung dịch là
A. NH4+, NO3-, HCO3-, OH-
B. K+, H+, SO42-, OH-
C. Na+, NH4+, H+, CO32-
D. Ca2+, Fe2+, NO3-, Cl-
-
Câu 5:
Cho dãy các chất sau: HCl, H2SO4, H3PO4, NaOH, C2H5OH, Ba(OH)2, Fe(NO3)3, NH4Cl, KAlO2. Số chất điện li mạnh là
A. 6
B. 7
C. 8
D. 9
-
Câu 6:
Cho các chất sau: KOH, Ca(OH)2, Al(OH)3, Zn(OH)2, Sn(OH)2 và Pb(OH)2. Số chất có tính chất lưỡng tính là
A. 2
B. 3
C. 4
D. 5
-
Câu 7:
Cho các phản ứng hóa học sau:
(1) (NH4)2SO4 + BaCl2
(2) CuSO4 + Ba(NO3)2
(3) Na2SO4 + BaCl2
(4) H2SO4 + BaSO3
(5) (NH4)2SO4 + Ba(OH)2
(6) Fe2(SO4)3 + Ba(NO3)2
Các phản ứng đều có cùng 1 phương trình ion rút gọn là
A. (1), (2), (3), (6)
B. (1), (3), (5), (6)
C. (2), (3), (4), (6)
D. (3), (4), (5), (6)
-
Câu 8:
Khối lượng kết tủa thu được khi trộn 10 ml dung dịch Na2SO4 1M và 10 ml dung dịch BaCl2 1M là
A. 1,79 gam
B. 2,33 gam
C. 3,94 gam
D. 4,39 gam
-
Câu 9:
Khi bị nhiệt phân dãy muối nitrat sau đây cho sản phẩm là kim loại, khí nitro dioxit và oxi?
A. AgNO3
B. Mg(NO3)2
C. KNO3
D. NH4NO3
-
Câu 10:
Cho 40 ml dung dịch HCl 0,75M vào 160 ml Ba(OH)2 0,1M. PH dung dịch thu được là
A. 2,5
B. 0,96
C. 12
D. 1
-
Câu 11:
Khi trộn 100 ml dung dịch Ba(OH)2 0,125M với 400 ml dung dịch HCl 0,05M thu được dung dịch có pH là
A. 2
B. 6
C. 10
D. 12
-
Câu 12:
Cho sơ đồ điều chế HNO3 trong phòng thí nghiệm:
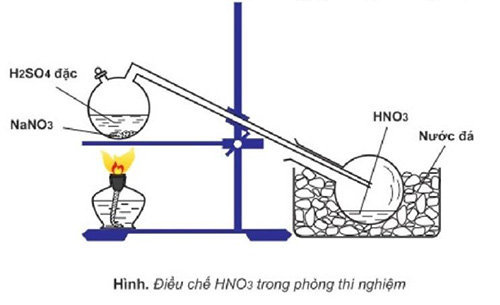
Phát biểu nào sau đây là sai khi nói về quá trình điều chế HNO3
A. Đốt nóng bình cầu bằng đèn cồn để phản ứng xảy ra nhanh hơn
B. HNO3 sinh ra dưới dạng hơi nên cần làm lạnh để ngưng tụ
C. HNO3 là axit yếu hơn H2SO4 nên bị đẩy ra khỏi muối
D. HNO3 có nhiệt độ sôi thấp (83o C) nên dễ bay hơi khi đun nóng
-
Câu 13:
Thể tích dung dịch HNO3 0,3M vừa đủ để trung hòa 100 ml dung dịch chứa hỗn hợp NaOH 0,1M và Ba(OH)2 0,1M là
A. 100 ml
B. 150 ml
C. 200 ml
D. 250 ml
-
Câu 14:
Trong phòng thí nghiệm, khí oxi có thể thu được bằng cách nhiệt phân KNO3. Đem nhiệt phân hoàn toàn 15,15 gam KNO3 thu được bao nhiêu lít khí O2
A. 1,86 lít
B. 3,36 lít
C. 2,24 lít
D. 1,68 lít
-
Câu 15:
Chọn câu đúng
A. Giá trị pH tăng thì độ axit giảm
B. Dung dịch có pH >7 làm quỳ tím hoá đỏ.
C. Dung dịch có pH < 7 làm quỳ tím hoá xanh.
D. Giá trị pH tăng thì độ axit tăng.
-
Câu 16:
Phát biểu nào sau đây không đúng
A. Đốt cháy NH3 trong không khí (xúc tác Pt) tạo khí không màu hóa nâu trong không khí
B. NH3 cháy trong oxi tỏa nhiều nhiệt nên được sử dụng là nhiên liệu tên lửa
C. Nhỏ vài giọt dung dịch phenol phtalein vào dung dịch NH3 thấy dung dịch chuyển sang màu hồng
D. Cho dung dịch NH3 từ từ vào dung dịch AlCl3 thấy xuất hiện kết tủa trắng không tan trong NH3
-
Câu 17:
Tiến hành thí nghiệm sau:
(1) Sục khí SO2 vào dung dịch H2S
(2) Cho mẫu Na vào dung dịch CuSO4
(3) Cho dung dịch AgNO3 vào dung dịch NaCl
(4) Sục khí NH3 tới dư vào dung dịch AlCl3
(5) Sục khí CO2 tới dư vào dung dịch Ca(OH)2
(6) Sục khí H2S tới dư vào dung dịch Pb(NO3)2
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa
A. 3
B. 5
C. 4
D. 2
-
Câu 18:
Cho dung dịch NaOH dư vào 300 ml dung dịch NH4Cl 1M, đun nóng nhẹ. Thể tích khí thu được là
A. 13,44 lít
B. 6,72 lít
C. 26,88 lít
D. 3,36 lít
-
Câu 19:
Hòa tan các chất KOH, C2H5OH, C12H22O11, NaCl vào nước để thu được các dung dịch riêng rẽ. Trong các dung dịch thu được có bao nhiêu dung dịch có khả năng dẫn điện
A. 3
B. 2
C. 1
D. 4
-
Câu 20:
Chất nào sau đây là chất điện li mạnh
A. HNO2
B. HF
C. Al2(SO4)3
D. CH3COOH
-
Câu 21:
Phản ứng nào sau đây có phương trình ion rút gọn là
H+ + OH‒ → H2O
A. Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
B. HCOOH + NaOH → HCOONa + H2O
C. HCl + NaOH → NaCl + H2O
D. 2NaOH + H2S → Na2S + 2H2O
-
Câu 22:
Chất nào sau đây là muối trung hòa
A. Fe2(SO4)3
B. NaHCO3
C. KHSO4
D. NaH2PO4
-
Câu 23:
Dãy muối nitrat nào sau đây khi bị nhiệt phân cho sản phẩm là oxit kim loại, khí nitơ đioxit và oxi?
A. Cu(NO3)2, AgNO3, NaNO3
B. KNO3, Hg(NO3)2, LiNO3
C. Pb(NO3)2, Zn(NO3)2, Cu(NO3)2.
D. Mg(NO3)2, Fe(NO3)3, AgNO3.
-
Câu 24:
Cho 100 ml dung dịch Ba(OH)2 nồng độ 0,1M vào 1 lít dung dịch (NH4)2CO3 0,01M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng dung dịch giảm là
A. 2,31 gam
B. 1,97 gam
C. 2,14 gam
D. 0,17 gam
-
Câu 25:
Phát biểu nào sau đây đúng
A. Khi tác dụng với kim loại hoạt động, N2 thể hiện tính khử
B. Sấm chớp trong các trận mưa dông có thể tạo ra khí N2O do N2 tác dụng với O2
C. Nito không duy trì sự hô hấp do nito là khí độc
D. Vì phân tử N2 có liên kết 3 rất bền nên ở nhiệt độ thường N2 khá trơ về mặt hóa học
-
Câu 26:
Cho 24,4 gam hỗn hợp Na2CO3, K2CO3 tác dụng vừa đủ với dung dịch BaCl2. Sau phản ứng thu được 39,4 gam kết tủa. Lọc tách kết tủa, cô cạn thu được bao nhiêu gam muối clorua khan?
A. 6,26 gam
B. 2,66 gam
C. 26,6 gam
D. 22,6 gam
-
Câu 27:
Cho 200 ml dung dịch NaOH 0,1M vào 100ml dung dịch HCl 0,5M. Dung dịch thu được sau phản ứng làm
A. Qùy tím không đổi màu
B. Phenol phtalein không màu chuyển sang màu hồng
C. Qùy tím hóa xanh
D. Qùy tím hóa đỏ
-
Câu 28:
Dẫn khí NH3 vào nước thu được dung dịch có tính
A. Bazo
B. Axit
C. Lưỡng tính
D. Trung tính
-
Câu 29:
Cho dãy các chất (NH4)2CO3; Al(OH)3; Zn(OH)2; NaHCO3; Na2SO4. Số chất trong dãy có khả năng vừa phản ứng với dung dịch HCl vừa phản ứng với dung dịch NaOH là?
A. 5
B. 4
C. 3
D. 2
-
Câu 30:
Cho các dung dịch HNO3, CH3COOH, NaCl, NaOH có cùng nồng độ mol, dung dịch nào có pH nhỏ nhất
A. HNO3.
B. CH3COOH.
C. NaCl.
D. NaOH.
-
Câu 31:
Cho 1,86 gam hỗn hợp gồm Al, Mg tác dụng với dung dịch HNO3 loãng dư thu được 560 ml khí N2O (sản phẩm khử duy nhất) bay ra. Khối lượng muối nitrat tạo ra trong dung dịch là
A. 40,5 gam
B. 14,62 gam
C. 24,16 gam
D. 14,26 gam
-
Câu 32:
Dung dịch X gồm 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl-; a mol Y2-. Cô cạn dung dịch X thu được m gam muối khan. Ion Y2- và giá trị của m là
A. SO42- và 56,5
B. CO32- và 42,1
C. CO32- và 30,1
D. SO42- và 37,3
-
Câu 33:
Số oxi hóa của nito được sắp xếp theo thứ tự tăng dần là
A. N2, NO, NH3, NO2-, NO3-
B. NO, N2O, NH3, NO3-, N2
C. NH3, N2, NH4+, NO, NO2
D. NH3, N2O, NO, NO2-, NO3-
-
Câu 34:
Dãy các chất đều tác dụng với dung dịch Ba(OH)2 là
A. NaHCO3, Na2CO3, CO2, MgSO4, HCl
B. Mg(NO3)2, HCl, BaCl2, NaHCO3, Na2CO3
C. NaHCO3, Na2CO3, CO2, Mg(NO3)2, Ba(NO3)2
D. Ba(NO3)2, Mg(NO3)2, HCl,CO2, Na2CO3
-
Câu 35:
Hòa tan 32 gam hỗn hợp Cu và CuO trong dung dịch HNO3 1M (dư) thoát ra 6,72 lít khí NO. Khối lượng CuO trong hỗn hợp ban đầu là
A. 2,52 gam
B. 1,88 gam
C. 3,2 gam
D. 1,2 gam
-
Câu 36:
Cho 2,16 gam Mg tác dụng với dung dịch HNO3 dư. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,896 lít khí NO ở điều kiện tiêu chuẩn và dung dịch X. Khối lượng muối khan thu được sau khi làm bay hơi dung dịch X là:
A. 8,88 gam
B. 13,32 gam
C. 6,52 gam
D. 13,92 gam
-
Câu 37:
Trong 1,5 lít dung dịch có hòa tan 0,3 mol NaCl. Nồng độ mol Na+; Cl- lần lượt là
A. 0,2M; 0,2M
B. 0,1M; 0,2M
C. 0,1M; 0,1M
D. 0,3M; 0,3M
-
Câu 38:
Cho V lít (đktc) hỗn hợp gồm N2; H2 có tỉ lệ mol là 1: 4 vào bình kín và đun nóng. Sau phản ứng được 1,5 mol NH3. Biết hiệu suất của phản ứng là H = 25%. Gía trị của V là
A. 42 lít
B. 268,8 lít
C. 336 lít
D. 448 lít
-
Câu 39:
Nung một lượng xác định muối Cu(NO3)2. Sau một thời gian dừng lại để nguội rồi đem cân thấy khối lượng giảm 54 gam. Khối lượng Cu(NO3)2 bị phân hủy là
A. 69 gam
B. 87 gam
C. 94 gam
D. 141 gam
-
Câu 40:
Nung 2,23 gam hỗn hợp X gồm các kim loại Fe, Al, Zn, Mg trong oxi, sau một thời gian thu được 2,71 gam hỗn hợp Y. Hòa tan hoàn toàn Y vào dung dịch HNO3 dư, thu được 0,672 lít khí NO (sản phẩm khử duy nhất ở đktc). Số mol HNO3 đã phản ứng là:
A. 0,12
B. 0,14
C. 0,16
D. 0,18











