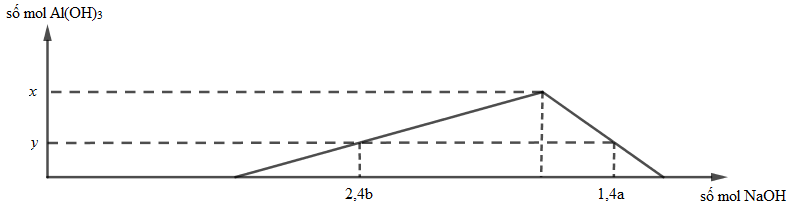
Cho từ từ đến dư dung dịch NaOH 0,1M vào 300 ml dung dịch hỗn hợp gồm H2SO4 a mol/lít và Al2(SO4)3 b mol/lít. Đồ thị dưới đây mô tả sự phụ thuộc của số mol kết tủa vào số mol NaOH đã dùng.
 Tỉ số a : b gần nhất với giá trị nào nhất sau đây?
Tỉ số a : b gần nhất với giá trị nào nhất sau đây?
Suy nghĩ trả lời câu hỏi trước khi xem đáp án
Lời giải:
Báo saiChọn B.
Theo đề: \({n_{{H_2}S{O_4}}}\; = 0,3a{\rm{ }}mol \Rightarrow {n_{{H^ + }}}\; = 0,6a{\rm{ }}mol\) và \({n_{A{l_2}{{(S{O_4})}_3}}}\; = 0,3b\;mol \Rightarrow {n_{A{l^{3 + }}}}\; = 0,6b{\rm{ }}mol.\)
Vì nH+ = 0,6a mol ⇒ nNaOH dùng để trung hòa = 0,6a mol.
+ Với 2,4b mol NaOH ta có: \({n_{Al{{(OH)}_3}}}\; = \;\frac{{2,4b - 0,6a}}{3} = y\) (1)
+ Với 1,4a mol NaOH ta có: \({n_{Al{{(OH)}_3}}}\; = 4{n_{A{l^{3 + }}}}--{n_{O{H^ - }}} = 4.0,6b--\left( {1,4a--0,6a} \right) = y{\rm{ }}\left( 2 \right)\)
+ Từ (1) và (2) ⇒ 0,8b – 0,2a = 2,4b – 0,8a \( \Leftrightarrow \frac{a}{b} = \frac{{1,6}}{{0,6}} = 2,667\)
Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020
Trường THPT Lê Văn Thọ











