Hòa tan hết 30,56 gam hỗn hợp gồm Mg, Fe3O4 và FeCO3 trong dung dịch chứa HCl và 0,24 mol HNO3, thấy thoát ra hỗn hợp khí X gồm CO2, NO và 0,08 mol N2O; đồng thời thu được dung dịch Y có khối lượng tăng 22,60 gam so với dung dịch ban đầu. Tỉ khối hơi của X so với He bằng 9,95. Cho dung dịch AgNO3 đến dư vào dung dịch Y, thu được 0,03 mol khí NO (sản phẩm khử duy nhất của N+5) và 239,66 gam kết tủa. Phần trăm khối lượng của Fe3O4 có trong hỗn hợp ban đầu là
Suy nghĩ trả lời câu hỏi trước khi xem đáp án
Lời giải:
Báo saiChọn D.
Khối lượng dung dịch tăng: \(30,56 - {m_X} = 22,6 \Rightarrow 44{n_{C{O_2}}} + 30{n_{NO}} = 4,44\) (1)
và \({n_X} = \frac{{{m_X}}}{{{M_X}}} = 0,2 \Rightarrow {n_{C{O_2}}} + {n_{NO}} = 0,12\) (2).
Từ (1), (2) có: \({n_{C{O_2}}} = {n_{NO}} = 0,06\;mol\)
\( \Rightarrow {n_{FeC{O_3}}} = 0,06\;mol \to {n_{N{H_4}^ + }} = 0,02\;mol\)
Khi đó: 24x + 232y + 0,06.116 = 30,56 (1)
Ta có: \({n_{{H^ + }}} = 10{n_{N{H_4}^ + }} + 2{n_{C{O_2}}} + 4{n_{NO}} + 10{n_{{N_2}O}} + 2{n_{O\;(F{e_3}{O_4})}} = {n_{HCl}} + {n_{HN{O_3}}} \Rightarrow {n_{HCl}} = 1,24 + 8y\)
Kết tủa thu được gồm AgCl (1,24 + 8y) và Ag (z mol) → 143,5.(1,24 + 8y) + 108z = 239,66 (2)
\( \to 2x + y + 0,06 = 0,09.3 + 0,08.8 + 0,02.8 + z\;\;(3)\)
Từ (1), (2), (3) suy ra: x = 0,5; y = 0,05; z = 0,04 → \(\% {m_{F{e_3}{O_4}}} = 37,96\% \) .
Đề thi thử tốt nghiệp THPT QG môn Hóa năm 2020
Trường THPT Lê Văn Thọ
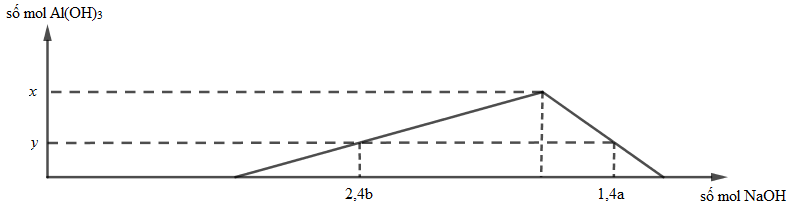 Tỉ số a : b gần nhất với giá trị nào nhất sau đây?
Tỉ số a : b gần nhất với giá trị nào nhất sau đây?










