850 câu trắc nghiệm môn Hóa học đại cương
Nhằm giúp các bạn ôn tập và hệ thống lại kiến thức nhanh chóng để đạt kết quả cao trong kì thi sắp tới, tracnghiem.net tổng hợp và chia sẻ đến các bạn 850 câu trắc nghiệm môn Hóa học đại cương, bao gồm các kiến thức tổng quan về các định luật và khái niệm cơ bản về hóa học, cấu tạo nguyên tử, bảng hệ thống tuần hoàn, liên kết hóa học, hiệu ứng nhiệt của các quá trình hóa học,cân bằng hóa học và mức độ diễn ra các quá trình hóa học,... Hi vọng sẽ trở thành nguồn tài liệu bổ ích giúp các bạn học tập và nghiên cứu một cách tốt nhất. Để ôn tập hiệu quả các bạn có thể ôn theo từng phần trong bộ câu hỏi này bằng cách trả lời các câu hỏi và xem lại đáp án và lời giải chi tiết. Sau đó các bạn hãy chọn mục "Thi thử" để hệ thống lại kiến thức đã ôn. Chúc các bạn thành công với bộ đề "Cực Hot" này nhé!
Chọn hình thức trắc nghiệm (45 câu/50 phút)
-
Câu 1:
Dựa vào độ âm điện của các nguyên tố: H = 2.1; C = 2.5; N = 3.0; O = 3.5. Hãy cho biết liên kết nào có cực nhiều nhất trong số các liên kết sau:
A. N−H
B. O−H
C. C−H
D. C−O
-
Câu 2:
Chọn phương án đúng: Phản ứng N2(k) + O2(k) ® 2NO(k) tỏa nhiệt. Tốc độ của phản ứng này sẽ tăng lên khi áp dụng các biện pháp sau: (1) Dùng xúc tác ; (2) Nén hệ; (3) Tăng nhiệt độ ; (4) Giảm áp suất hệ phản ứng.
A. 1, 3, 4
B. 2, 3, 4
C. 1, 2, 3
D. 1, 2
-
Câu 3:
Cân bằng trong phản ứng H2 (k) + Cl2 (k) ⇌ 2HCl (k) sẽ dịch chuyển theo chiều nào nếu tăng áp suất của hệ phản ứng?
A. Thuận
B. Nghịch
C. Không dịch chuyển
D. Không thể dự đoán
-
Câu 4:
Nguyên tử X có tổng số hạt proton, nơtron và electron là 36, số hạt không mang điện bằng nửa số hạt mang điện. Cấu hình e của nguyên tử X là:
A. 1s2 2s2 2p6
B. 1s2 2s2 2p6 3s1
C. 1s2 2s2 2p6 3s2
D. 1s2 2s2 2p6 3s2 3p6
-
Câu 5:
Cho một phản ứng thuận nghịch trong dung dịch lỏng A + B ⇌ C + D. Hằng số cân bằng Kc ở điều kiện cho trước bằng 200. Một hỗn hợp có nồng độ CA = CB = 10-3M, CC = CD = 0,01M. Trạng thái của hệ ở điều kiện này:
A. Hệ đang dịch chuyển theo chiều nghịch.
B. Hệ nằm ở trạng thái cân bằng.
C. Hệ đang dịch chuyển theo chiều thuận.
D. Không thể dự đoán được trạng thái của phản ứng.
-
Câu 6:
Chọn phương án đúng: Nguyên tố X ở chu kỳ IV, phân nhóm VIIB. Nguyên tố X có:
A. Z = 25, là phi kim loại
B. Z = 24, là kim loại
C. Z = 25, là kim loại
D. Z = 26, là phi kim loại
-
Câu 7:
Chọn đáp án đúng và đầy đủ nhất: Một phản ứng có DG298 > 0. Những biện pháp nào khi áp dụng có thể làm phản ứng xảy ra được: (1) Dùng xúc tác ; (2) Thay đổi nhiệt độ ; (3) Tăng nồng độ tác chất ; (4) Nghiền nhỏ các tác chất rắn.
A. 3, 4
B. 1, 3, 4
C. 2, 3
D. 1, 2, 3, 4
-
Câu 8:
Chọn phương án đúng: Cho 7N, 8O. Cấu hình electron hóa trị của phân tử NO+ là (x là trục liên kết ):
A. \({\left( {{\sigma _{2s}}} \right)^2}{\left( {\sigma _{2s}^ + } \right)^2}{\left( {{\pi _{2{p_x}}}{\pi _{2{p_y}}}} \right)^4}{\left( {{\sigma _{2{p_x}}}} \right)^2}\)
B. \({\left( {{\sigma _{2s}}} \right)^2}{\left( {\sigma _{2s}^ + } \right)^2}{\left( {{\pi _{2{p_y}}}} \right)^2}{\left( {{\sigma _{2{p_x}}}} \right)^2}{\left( {{\pi _{2{p_y}}}} \right)^2}\)
C. \({\left( {{\sigma _{2s}}} \right)^2}{\left( {\sigma _{2s}^ + } \right)^2}{\left( {{\pi _{2{p_x}}}{\pi _{2{p_y}}}} \right)^4}{\left( {{\sigma _{2{p_x}}}} \right)^1}{\left( {\pi _{2{p_y}}^ + } \right)^1}\)
D. \({\left( {{\sigma _{2s}}} \right)^2}{\left( {\sigma _{2s}^ + } \right)^2}{\left( {{\sigma _{2{p_x}}}} \right)^2}{\left( {{\pi _{2{p_x}}}{\pi _{2{p_y}}}} \right)^4}\)
-
Câu 9:
Chọn quá trình đúng: Xét phản ứng: NO(k) + ½O2(k) = NO2(k). Phản ứng được thực hiện trong xilanh với pistong chịu một áp suất không đổi, sau đó phản ứng được đưa về nhiệt độ ban đầu. Quá trình như thế là quá trình:
A. Đẳng tích, đẳng nhiệt
B. Đẳng tích, thể tích giảm
C. Đẳng áp, đẳng nhiệt
D. Đẳng áp, thể tích tăng
-
Câu 10:
Chọn phương án đúng: Dựa trên cấu hình electron hóa trị dưới đây, cho biết vị trí (chu kỳ, phân nhóm) của nguyên tố trong bảng hệ thống tuần hoàn: (1) 4d105s1 ; (2) 4f66s2 ; (3) 4s1.
A. 1: CK 5, PN: IB; 2: CK 6, PN: IIA; 3: CK 4, PN: IA
B. 1: CK 5, PN: IB; 2: CK 6, PN: IIIB; 3: CK 4, PN: IA
C. 1: CK 5, PN: IA; 2: CK 6, PN: IIIB; 3: CK 4, PN: IB
D. 1: CK 5, PN: IA; 2: CK 6, PN: VIIIB; 3: CK 4, PN: IA
-
Câu 11:
Chọn câu đúng: Dựa trên nguyên tắc xây dựng bảng HTTH, hãy dự đoán số nguyên tố hóa học tối đa có ở chu kỳ 8 (nếu có)
A. 32
B. 18
C. 50
D. 64
-
Câu 12:
Chọn phương án đúng. Nguyên tố X là kim loại, ở trạng thái oxi hóa dương cao nhất nó tạo được oxit có dạng X2O7. Trong nguyên tử X có 4 lớp electron. Xác định số thứ tự của X trong bảng hệ thống tuần hoàn:
A. 25
B. 35
C. 43
D. 17
-
Câu 13:
Chọn phương án đúng: Trong liên kết Van der Waals của hợp chất CH4 thì tương tác nào là đáng kể:
A. Không có cơ sở để xác định.
B. Tương tác định hướng.
C. Tương tác khuếch tán.
D. Tương tác cảm ứng.
-
Câu 14:
Trong các ký hiệu phân lớp lượng tử sau đây ký hiệu nào đúng?
A. 1s, 3d, 4s, 2p, 3f
B. 2p, 3s ,4d, 2d, 1p
C. 3g, 5f, 2p, 3d, 4s
D. 1s, 3d, 4f, 3p, 4d
-
Câu 15:
Chọn phương án đúng: Sơ đồ các pin hoạt động trên cơ sở các phản ứng oxy hóa khử:
3Ag+(dd) + Cr (r) = Cr3+(dd) + 3Ag(r)
2Fe2+(dd) + Cl2(k) = 2Fe3+(dd) + 2Cl-(dd) là:
A. (-) Cr½Cr3+(dd)∥Ag+(dd)½Ag(+) (-) Pt|Cl2(k)½Cl-(dd)∥ Fe2+(dd),Fe3+(dd)½Pt (+)
B. (-) Ag½Ag+(dd)∥Cr3+(dd)½Cr(+) (-) Pt½Fe2+(dd),Fe3+(dd)∥ Cl-(dd)½Cl2 | Pt (+)
C. (-) Cr½Cr3+(dd)∥Ag+(dd)½Ag(+) (-) Pt½Fe2+(dd), Fe3+(dd)∥ Cl-(dd)½Cl2| Pt (+)
D. (-) Ag½Ag+(dd)∥Cr3+(dd)½Cr(+) (-) Pt |Cl2(k)½Cl-(dd)∥ Fe2+(dd),Fe3+(dd)½Pt (+)
-
Câu 16:
Chọn câu sai: Ngược lại với NaCl, LiI tan nhiều trong rượu, tan ít trong nước, nhiệt độ nóng chảy thấp. Lí do là vì:
A. Liên kết trong phân tử LiI mang nhiều đặc tính cộng hóa trị, trái lại liên kết trong phân tử NaCl mang nhiều đặc tính ion.
B. LiI có khối lượng phân tử lớn hơn NaCl.
C. Ion Li+ có bán kính nhỏ hơn ion Na+, trong khi ion I- có bán kính lớn hơn ion Cl- nên sự phân cực của các ion trong LiI mạnh hơn.
D. Liên kết Li–I ít phân cực hơn liên kết Na–Cl.
-
Câu 17:
Chọn trường hợp đúng: Cho biết tích số tan của AgCl ở 250C là 10–10. (1) Độ tan của AgCl trong nước nguyên chất là 10–5 mol/l. (2) Độ tan của AgCl trong dung dịch KCl 0,1M giảm đi 107 lần so với trong nước nguyên chất. (3) Độ tan của AgCl trong nước sẽ ít hơn trong dung dịch KI 0,1M. (4) Độ tan của AgCl trong dung môi benzen sẽ lớn hơn trong dung môi nước.
A. 1, 2
B. 2, 4
C. 1, 3
D. 1, 3, 4
-
Câu 18:
Chọn phương án đúng: Một lít dung dịch chứa 5g muối ăn NaCl và 1 lít dung dịch chứa 20g đường C6H12O6. Cho biết khối lượng nguyên tử của Na, Cl, C, O, H lần lượt là 23; 35,5; 12; 16; 1. Giả sử độ điện ly của dung dịch muối là 1. Ở cùng nhiệt độ:
A. Dung dịch muối có nhiệt độ bắt đầu đông đặc cao hơn
B. Không thể so sánh được vì khác nhau về nồng độ và bản chất chất tan
C. Dung dịch đường có nhiệt độ bắt đầu sôi cao hơn
D. Dung dịch muối có áp suất thẩm thấu lớn hơn
-
Câu 19:
Tính pH của dung dịch chứa NH2OH và [NH3OH]Cl với tỷ lệ mol 2:1, biết \({K_{N{H_2}OH}} = {10^{ - 7.91}}\)
A. 6,09
B. 6,39
C. 5,79
D. 6,93
-
Câu 20:
Chọn câu sai trong các phát biểu sau về hợp chất ion:
A. Dẫn nhiệt kém.
B. Nhiệt độ nóng chảy cao.
C. Phân ly thành ion khi tan trong nước.
D. Dẫn điện ở trạng thái tinh thể.
-
Câu 21:
Chọn câu sai:
A. Các electron lớp bên trong có tác dụng chắn mạnh đối với các electron lớp bên ngoài
B. Các electron trong cùng một lớp chắn nhau yếu hơn so với khác lớp
C. Các electron lớp bên ngoài hoàn toàn không có tác dụng chắn với các electron lớp bên trong
D. Các electron trong cùng một lớp, theo chiều tăng giá trị ℓ sẽ có tác dụng chắn giảm dần
-
Câu 22:
Chọn phương án đúng: Tính hiệu ứng nhiệt DH0 của phản ứng: B ® A, biết hiệu ứng nhiệt của các phản ứng sau: C ® A: DH1 ; D ® C: DH2 ; D ® B DH3.
A. DH0 = DH3 + DH2 - DH1
B. DH0 = DH1 + DH2 + DH3
C. DH0 = DH1 + DH2 - DH3
D. DH0 = DH1 - DH2 - DH3
-
Câu 23:
Trong các phản ứng sau, trường hợp nào là hệ dị thể:
1) C6H5ONa(dd) + HCl(dd) = C6H5OH(ℓ) + NaCl(dd)
2) 2NaOH(dd) + H2SO4(dd) = Na2SO4(dd) + 2H2O(ℓ)
3) CH3COOCH3(dd) + H2O(ℓ) = CH3COOH(dd) + CH3OH(dd)
4) 2Al(r) + Fe2O3(r) = Al2O3(r) + 3Fe(r)
5) C (kim cương) = C (graphit)
A. 1, 2, 3
B. 2, 3, 5
C. 1, 4, 5
D. 1, 2, 3, 4, 5
-
Câu 24:
Chọn phương án đúng: Ocbital nguyên tử là: (1) hàm sóng mô tả trạng thái của electron trong nguyên tử được xác định bởi ba số lượng tử n, ℓ và mℓ. (2) bề mặt có mật độ electron bằng nhau của đám mây electron. (3) quỹ đạo chuyển động của electron trong nguyên tử. (4) đặc trưng cho trạng thái năng lượng của electron trong nguyên tử. (5) vùng không gian gần hạt nhân, trong đó xác suất có mặt của electron là 100%.
A. Chỉ phương án 1 đúng
B. Tất cả cùng đúng
C. Các phương án 2, 3 và 4 đúng
D. Các phương án 1 và 5 đúng
-
Câu 25:
Chọn câu đúng. Phản ứng: 2A(r) + B(ℓ) = 2C(r) + D(ℓ) có:
A. DS = 0
B. DS » 0
C. DS > 0
D. DS < 0
-
Câu 26:
Chọn phương án đúng: Khả năng tạo số liên kết cộng hóa trị cực đại của nguyên tố được quyết định bởi:
A. Số orbital nguyên tử ở lớp ngoài cùng.
B. Số electron hóa trị.
C. Số orbital nguyên tử hóa trị.
D. Số electron hóa trị độc thân ở trạng thái kích thích.
-
Câu 27:
Chọn nhóm các phân tử và ion có trạng thái lai hóa của nguyên tử trung tâm giống nhau: 1) CH4, SiH4, CCl4, NH4+, SO42-. 2) SO2, NO2, CO2, SiO2, ClO2. 3) CH4, SiF4, CH3Cl, CH2Cl2. 4) CH4, NH3, PCl3, H2O, NF3.
A. 1, 2, 3
B. 1, 3, 4
C. 1, 2, 3, 4
D. 2, 3
-
Câu 28:
Chọn câu sai: Theo thuyết MO:
1) Chỉ tồn tại các phân tử có bậc liên kết là một số nguyên.
2) Không tồn tại các phân tử sau: He2, Be2, Ne2.
3) Chỉ có các electron hóa trị của các nguyên tử mới tham gia tạo liên kết.
4) Các phân tử hoặc ion chỉ có electron ghép đôi thì nghịch từ.
5) Liên kết cộng hóa trị chỉ có kiểu liên kết σ và π mà không có kiểu liên kết δ.
A. 1, 3, 5
B. 1, 2, 5
C. 2, 3, 4
D. 1, 4, 5
-
Câu 29:
Chọn phát biểu đúng: (1) Acid càng yếu thì pKa càng lớn. (2) Dung dịch một base yếu có pH càng nhỏ khi pKb của nó càng lớn. (3) Base càng mạnh khi pKb càng lớn. (4) Giữa pKa và pKb của các dạng acid và base của H2PO4- có pKa + pKb = 14.
A. 2, 3
B. 1, 2
C. 1, 3, 4
D. 1, 2, 4
-
Câu 30:
Trong giản đồ sau, đường biểu diễn cân bằng Rắn ⇌ Khí là:
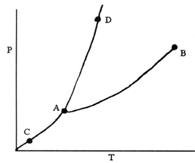
A. AC
B. AB
C. CD
D. AD
-
Câu 31:
So sánh góc liên kết trong các hợp chất cộng hóa trị sau: 1) NH3 ; 2) NF3 ; 3) NI3 ; 4) CO2.
A. 3 < 1 < 2 < 4
B. 4 < 1 < 3 < 2
C. 2 < 3 < 1 < 4
D. Không so sánh được
-
Câu 32:
Chọn câu phù hợp nhất. Cho phản ứng 2Mg (r) + CO2 (k) = 2MgO (r) + Cgraphit. Phản ứng này có hiệu ứng nhiệt tiêu chuẩn \(\Delta H_{298}^0\) = -822,7 kJ , \(\Delta S_{298}^0\) = -219,35J/K. Về phương diện nhiệt động hóa học, phản ứng trên có thể: (Cho biết so với các chất trong phản ứng, MgO là chất có nhiệt độ nóng chảy cao nhất là 2800°C)
A. Không xảy ra tự phát ở nhiệt độ cao.
B. Xảy ra tự phát ở nhiệt độ cao.
C. Xảy ra tự phát ở nhiệt độ thấp.
D. Xảy ra tự phát ở mọi nhiệt độ.
-
Câu 33:
Chọn phương án đúng: Cho: 12Mg, 17Cl, 20Ca, 26Fe, 80Hg. So sánh độ ion của mỗi cặp hợp chất sau: (FeCl2 và FeCl3) ; (FeCl2 và MgCl2) ; (CaCl2 và HgCl2)
A. FeCl2 > FeCl3 ; FeCl2 < MgCl2 ; CaCl2 > HgCl2
B. FeCl2 < FeCl3 ; FeCl2 < MgCl2 ; CaCl2 < HgCl2
C. FeCl2 > FeCl3 ; FeCl2 < MgCl2 ; CaCl2 < HgCl2
D. FeCl2 < FeCl3 ; FeCl2 > MgCl2 ; CaCl2 > HgCl2
-
Câu 34:
Cho hai nguyên tử với các phân lớp electron ngoài cùng là: X(3s23p1) và Y(2s22p4). Công thức phân tử của hợp chất giữa X và Y có dạng nào dưới đây:
A. XY2
B. XY3
C. X2Y3
D. X3Y
-
Câu 35:
Chọn câu sai trong các phát biểu sau về các hợp chất ion:
A. Khả năng phân ly tạo ion không phụ thuộc vào bản chất dung môi mà chỉ phụ thuộc bản chất hợp chất ion.
B. Dễ phân ly thành ion trong nước.
C. Không dẫn điện ở trạng thái tinh thể.
D. Dẫn điện ở trạng thái nóng chảy.
-
Câu 36:
Chọn ra câu đúng:
A. Tất cả nguyên tố thuộc hai họ Lantanid và Actinid đều có số oxy hóa dương lớn nhất là +3
B. Số oxy hóa dương lớn nhất của nhóm IB là +1
C. Số oxy hóa âm thấp nhất của nhóm VIIB là -1
D. Tất cả nguyên tố thuộc hai họ Lantanid và Actinid đều là nguyên tố f
-
Câu 37:
Một bình bằng thép dung tích 10 lít chứa đầy khí H2 ở (0°C, 10 atm) được dùng để bơm các quả bóng. Nhiệt độ lúc bơm giữ không đổi ở 0°C. Nếu mỗi quả bóng chứa được 1 lít H2 ở đktc thì có thể bơm được bao nhiêu quả bóng?
A. 90 quả
B. 100 quả
C. 1000 quả
D. 10 quả
-
Câu 38:
Chọn phát biểu sai theo thuyết MO:
A. MO p có mặt phẳng phản đối xứng chứa trục liên kết.
B. Phân tử là tổ hợp thống nhất của các hạt nhân nguyên tử và các electron, trạng thái electron được đặc trưng bằng hàm số sóng phân tử.
C. Trong phân tử, các electron của nguyên tử chịu lực tác dụng của tất cả hạt nhân nguyên tử.
D. Các orbital phân tử được tạo thành do sự tổ hợp tuyến tính các orbital nguyên tử, số MO tạo thành có thể khác số AO tham gia tổ hợp.
-
Câu 39:
Chọn dãy các chất có cùng trạng thái lai hóa của nguyên tử trung tâm. (1) CH2Cl2, NF3, ClOF, SO42- ; (2) SO2Cl2, H2O, NH4+, O(C2H5)2 ; (3) NO2, NO3-, SO2, O3 ; (4) H2CO, OC(NH2)2, CO32-, CO(CH3)2.
A. 2, 3
B. 4
C. 1, 2, 3
D. 1, 2, 3, 4
-
Câu 40:
Chọn phương án đúng: Cho biết số electron tối đa và số lượng tử chính n của các lớp lượng tử O và Q:
A. lớp O: 72e, n=6; lớp Q: 49e, n = 7
B. lớp O: 50e, n=5; lớp Q: 36e, n = 6
C. lớp O: 32e, n=4; lớp Q: 72e, n = 6
D. lớp O: 50e, n=5; lớp Q: 98e, n = 7
-
Câu 41:
Chọn phát biểu đúng về dung dịch rắn:
A. Dung dịch rắn thay thế và dung dịch rắn xen kẽ được xác định dựa vào cách bố trí các tiểu phân trong mạng tinh thể.
B. Dung dịch rắn xen kẽ và dung dịch rắn thay thế đều là các dung dịch rắn hạn chế.
C. Tất cả các chất đều tạo được dung dịch rắn với nhau khi chúng có kiểu mạng tinh thể gần nhau.
D. Trong thực tế, không tồn tại dung dịch rắn liên tục.
-
Câu 42:
Chọn phương án đúng: Xét các phân tử và ion sau: \(O_2^ + ,{O_2},O_2^ - ,O_2^{2 - }\)
1) Ion \(O_2^{2 - }\) nghịch từ.
2) Độ bền liên kết tăng dần từ trái sang phải.
3) Độ dài liên kết tăng dần từ trái sang phải.
4) Bậc liên kết tăng dần từ trái sang phải.
A. 2, 4
B. 1, 2, 4
C. 1, 3
D. 2, 3
-
Câu 43:
Chọn phương án đúng: Trong dãy hợp chất với hydro của các nguyên tố nhóm VIA: H2O, H2S, H2Se, H2Te, nhiệt độ sôi các chất biến thiên như sau:
A. Tăng dần từ H2O đến H2Te.
B. Chúng có nhiệt độ sôi xấp xỉ nhau vì có cấu trúc phân tử tương tự nhau.
C. Không so sánh được vì độ phân cực của chúng khác nhau.
D. Nhiệt độ sôi của H2O > H2S < H2Se < H2Te (nhiệt độ sôi của H2S thấp nhất).
-
Câu 44:
Chọn phương án đúng: Khi ghép một tấm bạc trong dung dịch bão hòa AgBr và một tấm bạc khác trong dung dịch AgNO3 0,01M ta được pin nồng độ có suất điện động ở 250C là 0,245V. Hãy tính tích số tan của AgBr ở 250C.
A. 2 ×10-12
B. 2 ×104
C. 5 ×10-13
D. Không đủ dữ liệu để tính
-
Câu 45:
Cho các phản ứng:
(1) N2 (k) + O2 (k) ⇌ 2NO (k) DH° > 0
(2) N2 (k) + 3H2 (k) ⇌ 2NH3 (k) DH° < 0
(3) MgCO3 (r) ⇌ MgO (r) + CO2 (k) DH° > 0
Với phản ứng nào ta nên dùng nhiệt độ cao và áp suất thấp để cân bằng chuyển dịch theo chiều thuận.
A. Phản ứng (1)
B. Phản ứng (3)
C. Phản ứng (2)
D. Phản ứng (1) và (2)