Trắc nghiệm Cấu trúc lớp vỏ electron nguyên tử Hóa Học Lớp 10
-
Câu 1:
Trong tự nhiên, đồng vị phổ biến nhất của hiđro là đồng vị nào dưới đây?
-
Câu 2:
Cấu hình electron phân lớp ngoài cùng của các nguyên tử R, X, Y lần lượt là 2p4, 3s1, 3p1. Phân tử hợp chất ion đơn giản giữa X và R, giữa Y và R lần lượt có số hạt mang điện là
-
Câu 3:
Cho cấu hình electron của các nguyên tử sau
:\(\begin{array}{l} (X)1{s^2}2{s^2}2{p^6}3{s^2}3{p^3}\\ (Y)1{s^2}2{s^2}2{p^6}3{s^2}3{p^6}4{s^1}\\ (Z)1{s^2}2{s^2}2{p^6}3{s^2}\\ (T)1{s^2}2{s^2}2{p^6}3{s^2}3{p^6}3{d^8}4{s^2} \end{array}\)
Dãy các cấu hình electron của các nguyên tử kim loại là
-
Câu 4:
Trong phân tử N2, số cặp electron dùng chung là (cho 7N)
-
Câu 5:
Biết nguyên tử cacbon gồm: 6 proton, 6 nơtron và 6 electron, khối lượng 1 mol nguyên tử cacbon là
-
Câu 6:
Trong nguyên tử X các e được phân bố trên 3 lớp, lớp thứ 3 có 8e. Điện tích hạt nhân của nguyên tử X là
-
Câu 7:
Có các đồng vị sau \({}_1^1H;\;{}_1^2H;\;{}_{17}^{35}Cl;{}_{17}^{37}Cl\). Có thể tạo ra số phân tử hiđroclorua HCl là
-
Câu 8:
Nguyên tử photpho có 15 proton, 16 nơtron và 15 electron, khối lượng của 1 nguyên tử photpho là
-
Câu 9:
Có các nguyên tố hóa học: Cr (Z = 24), Fe (Z = 26), P (Z = 15), Al (Z =13). Nguyên tố mà nguyên tử của nó có số electron độc thân lớn nhất ở trạng thái cơ bản là
-
Câu 10:
Cho cấu hình electron nguyên tử của Fe (Z = 26) : \(1{s^2}2{s^2}2{p^6}3{s^2}3{p^6}3{d^6}4{s^2}\) . Fe thuộc loại nguyên tố
-
Câu 11:
Nguyên tử Na (Z = 11) bị mất đi một electron thì cấu hình electron của ion tạo thành là
-
Câu 12:
Có 3 nguyên tử: \({}_6^{12}X,\;{}_7^{14}Y,\;{}_6^{14}Z\). Những nguyên tử là đồng vị của cùng một nguyên tố hóa học là
-
Câu 13:
Trong tự nhiên, kali có 3 đồng vị : Biết nguyên tử khối trung bình của kali là 39,13. Giá trị của x2 và x3 lần lượt là
-
Câu 14:
Nguyên tử của nguyên tố T có cấu hình electron như sau: \(1{{\rm{s}}^2}2{{\rm{s}}^2}2{{\rm{p}}^6}3{{\rm{s}}^2}3{{\rm{p}}^6}3{{\rm{d}}^{10}}4{{\rm{s}}^2}.\)
Phát biểu nào sau đây không đúng?
-
Câu 15:
Nguyên tử của nguyên tố Z có 4 lớp electron, lớp ngoài cùng có 6 electron. Số hiệu nguyên tử của Z là
-
Câu 16:
Nguyên tố X có kí hiệu nguyên tử là \({{}_9^{19}X}\) Kết luận nào sau đây về cấu tạo nguyên tử X là đúng
.png)
-
Câu 17:
Khối lượng nguyên tử tập trung hầu hết ở hạt nhân và được tính gần đúng bằng
-
Câu 18:
Số electron độc thân trong nguyên tử oxi ở trạng thái cơ bản là:
-
Câu 19:
Cấu hình electron biểu diễn theo ô lượng tử nào dưới đây không đúng?
-
Câu 20:
Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm về số nguyên tử như sau:
.png)
Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg, thì số nguyên tử tương ứng của hai đồng vị 24, 26 lần lượt là bao nhiêu?
-
Câu 21:
Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm về số nguyên tử như sau:
.png)
Nguyên tử khối trung bình của Mg là
-
Câu 22:
Theo định nghĩa, số Avogađro là một số bằng số nguyên tử đồng vị 12C có trong 12 gam đồng vị 12C. Số Avogađro được kí hiệu là N, N có giá trị là ≈6,022.1023. Khối lượng của một nguyên tử 12C là bao nhiêu gam
-
Câu 23:
Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố X là 10. Số khối của nguyên tử X là
-
Câu 24:
Nguyên tử của nguyên tố R có 3 lớp e, lớp ngoài cùng có 3e. Vậy số hiệu nguyên tử của nguyên tố R là:
-
Câu 25:
Cấu hình electron lớp ngoài cùng của nguyên tử X phân bố như sau:
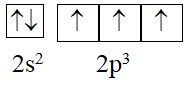
Số hiệu nguyên tử và kí hiệu nguyên tử X là
-
Câu 26:
Sắp xếp các nguyên tử sau theo thứ tự tăng dần số nơtron
-
Câu 27:
Cho ba nguyên tử có kí hiệu là \({}_{12}^{24}Mg,{}_{12}^{25}Mg,{}_{12}^{26}Mg\). Phát biểu nào sau đây là sai?
-
Câu 28:
Một nguyên tử có 17 electron. Số phân lớp electron của nguyên tử này là
-
Câu 29:
Một nguyên tử có 14 electron. Số electron p của nguyên tử này là
-
Câu 30:
Cho các nguyên tử:\({}_{11}^{23}X,\;{}_{19}^{39}Y,\;{}_{13}^{27}Z\). Phát biểu nào sau đây là đúng?
-
Câu 31:
Nguyên tử nào sau đây có 8 electron ở lớp ngoài cùng?
-
Câu 32:
Phân bố electron trên các lớp K/L/M/N của nguyên tố asen lần lượt là 2/8/18/5. Phát biểu nào sau đây là sai?
-
Câu 33:
Cho hai nguyên tố M và N có số hiệu nguyên tử lần lượt là 11 và 13. Cấu hình electron của M và N lần lượt là:
-
Câu 34:
Trong nguyên tử nguyên tố X có tổng số hạt proton , notron , electron là 34. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt. Số hiệu nguyên tử của X là
-
Câu 35:
Cho biết sắt có số hiệu nguyên tử là 26. Viết cấu hình electron của ion Fe2+
-
Câu 36:
Biết Cu có số hiệu nguyên tử là 29. Cấu hình electron của ion Cu+ là
-
Câu 37:
Cho số hiệu nguyên tử của các nguyên tố sau: Na(Z=11); K(Z=19); Ca(Z=20); Cl(Z=17). Ion nào sau đây có cấu hình electron 1s22s22p6?
-
Câu 38:
Cấu hình electron của ion nào sau đây không giống cấu hình của khí hiếm?
-
Câu 39:
Cho số hiệu nguyên tử của các nguyên tố O, K, Ca, Fe lần lượt là 8, 19, 20, 26. Cấu hình electron của ion nào sau đây không giống cấu hình của khí hiếm?
-
Câu 40:
Một nguyên tử của nguyên tố X có tổng số hạt proton, nơtron, electron là 155 và số khối là 108. Kí hiệu của nguyên tử X là
-
Câu 41:
Một nguyên tử của nguyên tố X có tổng số hạt proton, nơtron, electron là 52 và số khối là 35. Kí hiệu của nguyên tử X là
-
Câu 42:
Nguyên tử X có tổng số hạt p, n, e là 34 và số khối là 23. Số lớp electron và số electron lớp ngoài cùng lần lượt là
-
Câu 43:
Biết rằng tổng số hạt (proton, nơtron, electron) của một nguyên tử X là 20. Tổng số phân lớp electron trong nguyên tử của nguyên tố X là
-
Câu 44:
Một nguyên tử của nguyên tố X có tổng số hạt proton, nơtron, electron là 28 và số khối là 19. Số proton trong nguyên tử X là
-
Câu 45:
Nguyên tử X có tổng số hạt proton, nơtron, electron là 115 và số khối là 80. Số lớp electron và số electron ở lớp ngoài cùng của X lần lượt là
-
Câu 46:
Trong nguyên tử một nguyên tố X có 29 electron và 36 nơtron. Số khối và số lớp electron của nguyên tử X lần lượt là
-
Câu 47:
Nguyên tố X (thuộc nhóm A), có cấu hình electron lớp ngoài cùng của nguyên tử là 3s23p6. Cấu hình electron nguyên tử (đầy đủ) của X
-
Câu 48:
Nguyên tử của nguyên tố nào sau đây có cấu hình electron bất thường?
-
Câu 49:
Nguyên tử của một nguyên tố X có tổng số hạt cơ bản (proton, nơtron, và electron) là 82, biết số hạt mạng điện nhiều hơn số hạt không mang điện là 22. Kí hiệu hóa học của X là
-
Câu 50:
Một nguyên tử kim loại M khi nhường 2e ở lớp ngoài nó trở thành cation mang điện M2+. Biết M2+ có phân mức năng lượng cao nhất là 3p6. Vậy M có cấu hình e là











